權 寧博*,森脇知子**
*日本大学医学部内科学系呼吸器内科学分野
**アストラゼネカ株式会社メディカル本部呼吸器・免疫疾患領域部(〒530-0011 大阪府大阪市北区大深町3-1 グランフロント大阪タワーB 19F)
A new therapeutic goal for severe asthma: remission
Yasuhiro Gon *,Tomoko Moriwaki**
*Division of Respiratory Medicine, Department of Internal Medicine, Nihon University School of Medicine, Tokyo
**Medical, Respiratory & Immunology, AstraZeneca K.K., Osaka
Keywords:重症喘息,臨床的寛解,呼吸機能,生物学的製剤,全身性ステロイド薬/severe asthma, clinical remission, respiratory function, biologics, systemic corticosteroid
呼吸臨床 2023年7巻10号 論文No.e00180
Jpn Open J Respir Med 2023 Vol. 7 No. 10 Article No.e00180
DOI: 10.24557/kokyurinsho.7.e00180
受付日:2023年7月26日
掲載日:2023年10月16日
©️Yasuhiro Gon, et al. 本論文はクリエイティブ・コモンズ・ライセンスに準拠し,CC-BY-SA(原作者のクレジット[氏名,作品タイトルなど]を表示し,改変した場合には元の作品と同じCCライセンス[このライセンス]で公開することを主な条件に,営利目的での二次利用も許可されるCCライセンス)のライセンシングとなります。詳しくはクリエイティブ・コモンズ・ジャパンのサイト(https://creativecommons.jp/)をご覧ください。
喘息は気道の慢性炎症を本態とし,気道炎症や気道過敏性亢進によって生じる変動性を持った気道狭窄は喘鳴,呼吸困難,胸苦しさや咳などの臨床症状を引き起こす。持続する気道炎症は,気道粘膜の傷害とそれに引き続く気道構造の変化(気道リモデリング)を誘導し,非可逆的な気流制限の進行をもたらす。
喘息治療において抗炎症薬である吸入ステロイド薬(ICS)が果たした功績は大きく,ICSの普及により喘息のコントロールは格段に向上し,喘息死は大きく減少した。高用量ICSを使用してもコントロール不良である重症喘息の疾病負荷が大きな課題であったが,2009年以降,次々に登場した生物学的製剤により,重症喘息においても増悪の抑制,呼吸機能の改善,喘息症状の改善,経口ステロイド薬(OCS)減量などが達成可能なものとなってきた[1]。さらに,これら生物学的製剤は喘息病態形成にかかわる分子を標的としており,現在の症状コントロールのみならず,気道過敏性亢進の改善[2][3][4]や気道線維化にかかわる細胞外基質タンパク質沈着の抑制[5]など,疾患修飾に繋がるような報告も確認されている。
喘息と同じ慢性炎症性疾患である関節リウマチでは,病態の進展抑制効果を示す抗リウマチ薬を中心とした治療の進歩とともに,薬物治療の目標として寛解の概念が確立したことにより,長期的な臨床転帰の改善と患者のQOLの向上がもたらされた[6][7]。重症喘息においても病態の理解が進み,生物学的製剤による治療が普及した今,治療による寛解についての議論を深める良いタイミングではないだろうか。
本稿は,近年専門家らが発表した治療による喘息寛解についての提唱に基づき,重症喘息における寛解の概念を整理し,寛解を新たな治療目標として提案することで,よりよい重症喘息治療の一助となることを目的とする。
寛解とは広義には疾患活動性が低い,あるいはまったくない状態または期間と定義されている[8][9]。では喘息治療における寛解はどのように考えればよいだろうか。
2020年に公表されたMenzies-Gowらのコンセンサスレポート[10]において,包括的かつ実用的な喘息の寛解の定義は,症状のコントロールと将来リスクの回避からなる既存の治療目標を超越した概念であるべきと提言されている。彼らは,気道炎症の消失や呼吸機能の経年低下,気道リモデリングの抑制などの評価項目をこの定義に含めるべきとし,寛解の評価項目およびその基準を提唱した(図1)[10]。具体的には,①顕著な喘息症状なし,②呼吸機能の最適化および安定化,③患者と医療提供者が共に臨床的寛解を認める,および④増悪に対する処置および長期疾患管理のための全身性ステロイド薬(SCS)使用なし,以上の4項目が12カ月以上継続した状態を臨床的寛解と定義し,臨床的寛解に加え,⑤バイオマーカーなどにより喘息に関連する炎症の消失が客観的に評価できること,⑥気道過敏性が陰性であること,以上の6項目が12カ月以上継続した状態を完全寛解と定義している。
図1 寛解の評価項目およびその基準
喘息における寛解の一般的な枠組み。治療下,無治療下の臨床的寛解および完全寛解の基準は,臨床専門家のコンセンサスによって特定された。
(文献10より許可を得て転載)
これらの枠組みは,客観的および主観的な尺度に基づき,呼吸機能,炎症マーカー,増悪頻度,症状コントロールなど,疾患のすべての重要な側面を含んでおり,喘息の疾患活動性の複合的な評価が可能である。なお,完全寛解に至ったとしてもある程度の気道リモデリングが認められるため,正式には喘息の治癒とは言えない[11]。また,喘息の重症度は時間の経過および季節により変動している[12][13]。したがって,寛解状態に達した後も長期にわたって炎症や臨床症状を再評価するための継続的な定期フォローアップが必要であり,上述した通りMenzies-Gowらはその期間を12カ月以上と提唱している[10]。この寛解という概念は,長期的にその状態を維持するという観点から,ある特定の時点で評価されるトータルコントロールとは異なったものである。
喘息のガイドラインにおいては,2023年に世界で初めてドイツの喘息ガイドラインに,治療目標としての寛解が記載された[14]。Menzies-Gowらのコンセンサスレポートと同様,本ガイドラインにおいても,“寛解”という用語を,SCSの使用を認める短期的な“喘息コントロール”という用語とは対照的に,SCSを使用せず,長期にわたって喘息症状や増悪がなく,呼吸機能が安定している状態として説明されている。
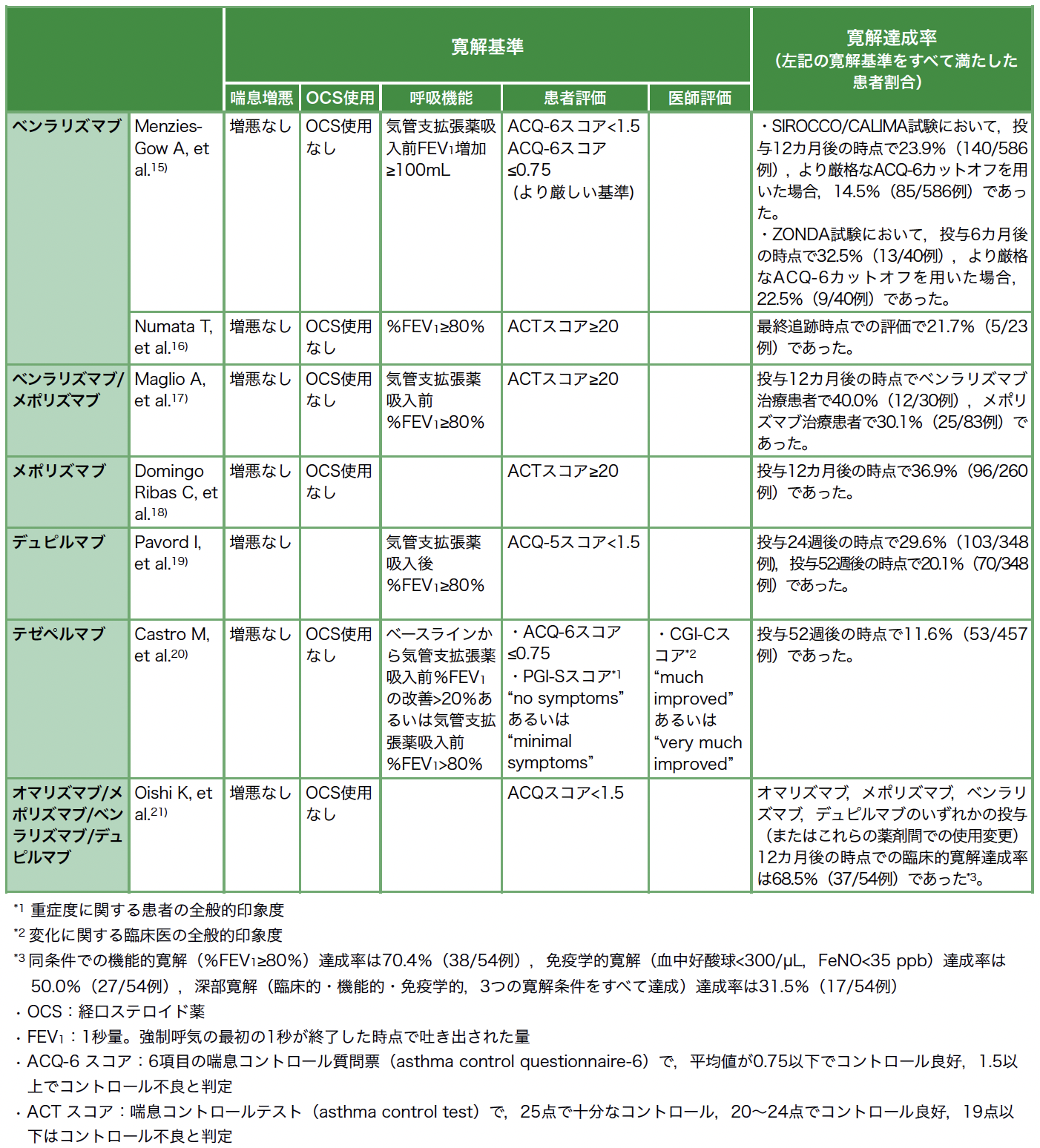
重症喘息において,現在の治療で完全寛解を達成するハードルは高いため,まずは臨床的寛解を目指すことが当面の目標となろう。また,実臨床において臨床的寛解を臨床医共通の目標とするためには,わかりやすくシンプルな評価項目が望ましい。実際に生物学的製剤を使用した臨床試験において,臨床的寛解を評価するためにどのような項目が採用されているかを整理した(表1)。
表1 重症喘息における生物学的製剤の有用性を検討した各臨床試験での寛解基準
いずれの報告においても“増悪なし”,“顕著な喘息症状なし”は共通した評価項目であり,これらの項目に関しては多くの臨床医の間で認識の齟齬はないと考える。また,OCSは気道炎症を効果的に抑制する一方,頻回にOCSが必要となる患者では,気道炎症が抑制しきれていないことが推測される。したがって,臨床的寛解の評価項目として“(長期管理薬および頓用としての)OCS使用なし”を含めることも重要であろう。
一方,呼吸機能に関しては意見が分かれるところではないだろうか。重症喘息患者では気道リモデリングが進んでいる患者もおり,健康な人と同じレベルまでの改善は難しいことが想定される。Menzies-Gowらの報告においても呼吸機能の‟正常化”とは言わず,‟最適化と安定化”という表現が使用されている[10]。呼吸機能の評価を最適化,安定化として捉え,臨床的寛解の評価項目とするのか,あるいは構造的観点からむしろ完全寛解の評価項目とするのかについては,さらなる議論が必要である。
臨床的寛解を目標とした場合においても,これまでの喘息コントロールを目指した喘息患者への対応と同様に,まずは感作アレルゲンやその他喫煙などの増悪因子の回避および除去に努め,吸入手技の指導やアドヒアランスの管理,合併疾患の管理を積極的に行うことが重要である。その上で,高用量のICSと長時間作用性β2刺激薬(LABA)に加え,患者のフェノタイプに応じて長時間作用性抗コリン薬(LAMA),ロイコトリエン受容体拮抗薬(LTRA),テオフィリン徐放性製剤の複数を併用して臨床的寛解を目指す。それでも臨床的寛解が達成されない場合,生物学的製剤による治療強化が検討される。喘息の発症年齢,バイオマーカー,合併症などから,個々の患者に適した生物学的製剤の選択を行うことが重要である。現在,生物学的製剤を用いて臨床的寛解に至る重症喘息患者の割合は11.6~68.5%[15]〜[21]と報告されている(表1)。各試験で報告されている割合にばらつきがある背景としては,臨床的寛解の評価項目として呼吸機能の扱い方の違いや,患者背景が異なることなどが考えられる。さらに,生物学的製剤による臨床的寛解達成に関連する因子として,短い喘息罹病期間,より高い呼吸機能などが確認されている[21][22]。このことから,重症喘息患者に対して,早期からの生物学的製剤の治療導入も重要な検討事項ではないだろうか。
さらに,臨床的寛解の評価項目達成後も,その状態を維持することが肝要である。日常診療下において,常に喘息治療の目標を医師と患者の間で共有すること,その上で臨床的寛解の意義を患者に説明することで,継続治療の理解向上を促し,その結果として良好なアドヒアランスの維持,治療の継続が期待される。