
舟口祝彦,豊吉沙耶香,石垣裕敏
朝日大学病院呼吸器内科(〒500-8523 岐阜県岐阜市橋本町3-23)
Pulmonary cryptococcosis in an older patient presenting with a giant mass: a case report
Norihiko Funaguchi, Sayaka Toyoshi, Hirotoshi Ishigaki
Department of Respiratory Medicine, Asahi University Hospital, Gifu
Keywords:肺クリプトコッカス症,クリプトコッカス髄膜炎,巨大腫瘤,ボリコナゾール/pulmonary cryptococcosis, cryptococcal meningitis, giant mass, voriconazole
呼吸臨床 2024年8巻3号 論文No. e00186
Jpn Open J Respir Med 2024 Vol. 8 No. 3 Article No.e00186
DOI: 10.24557/kokyurinsho.8.e00186
受付日:2024年1月12日
掲載日:2024年3月15日
©️Norihiko Funaguchi, et al. 本論文はクリエイティブ・コモンズ・ライセンスに準拠し,CC-BY-SA(原作者のクレジット[氏名,作品タイトルなど]を表示し,改変した場合には元の作品と同じCCライセンス[このライセンス]で公開することを主な条件に,営利目的での二次利用も許可されるCCライセンス)のライセンシングとなります。詳しくはクリエイティブ・コモンズ・ジャパンのサイト(https://creativecommons.jp/)をご覧ください。
肺クリプトコッカス症は,鳥類の糞便や土壌中に存在するCryptococcus(C.)neoformansや樹木や土壌に存在するC. gattiiを経気道的に吸入することにより感染する深在性真菌症である[1][2]。クリプトコッカス感染の背景となる基礎疾患には細胞性免疫の低下を引き起こす疾患であるhuman immunodeficiency virus(HIV)感染,移植後の免疫抑制状態,長期のステロイド使用,糖尿病などが挙げられる[3][4]。
肺クリプトコッカス症の画像所見は孤立結節,多発結節,浸潤影など多彩であり,肺癌,肺結核,肺炎・肺化膿症などとの鑑別が問題になることがある。肺クリプトコッカス症において本症例の様な巨大腫瘤を呈することは比較的稀であり,超高齢症例においてもvoriconazole(VRCZ)による治療が安全かつ有用であったため報告する。
症例:93歳,女性。
主訴:発熱,咳,意識障害。
既往歴:誤嚥性肺炎。
喫煙歴・飲酒歴:なし。
家族歴:45年前に夫が肺結核に罹患。
生活歴:鳥類の飼育・接触歴なし。
現病歴:慢性心不全,糖尿病,リウマチ性多発筋痛症で当院に通院中,リウマチ性多発筋痛症に対してX−1年5月よりprednisolone 5mg/日の内服中であった。X年6月になり徐々に食欲の低下を認めていた。7月になり38℃台の発熱,咳を認めるようになった。認知機能も徐々に低下してきていた。自宅で倒れて動けなくなっているのを家人が発見し,当院に救急搬送された。頭部外傷は認めなかったが,意識障害と胸部
異常陰影・呼吸不全を認めたため,当科に入院となった。
入院時現症:身長140cm,体重38kg,血圧94/38 mmHg,体温39.0℃,脈拍91回/分,室内気経皮酸素飽和度84%,呼吸数14回/分,意識レベルGlasgow Coma Scale 8点 E3V2M3,右肺呼吸音軽度減弱,表在リンパ節触知せず,項部硬直なし。
入院時検査所見:血液検査で白血球数は10,800/μLと増加,白血球分画では好中球86.6%と増加,リンパ球6.6%と減少。CRPは3.3mg/dLと上昇。HbA1c 7.7%と上昇していた。β-Dグルカン5.0pg/mL未満,Tスポット陰性,クリプトコッカス抗原陽性,HIV抗体は陰性であった(表1)。喀痰検査では抗酸菌塗抹・培養陰性,結核菌PCR陰性であった。
入院時胸部画像所見:入院時の胸部X線写真(図1a)では右上中肺野に腫瘤影および両肺野に小結節・結節状影の散在を認めた。胸部CT(図1b〜d)では右上葉S2に長径10cm大の腫瘤性病変および両肺野に多発小結節・結節影を認めた。脳MRIでは脳萎縮以外は明らかな異常所見は認めなかった。
図1 入院時胸部画像所見
胸部X線写真で右上中肺野に腫瘤影および両肺野に小結節・結節状影の多発する所見を認めた(a)。胸部CTでは右上葉S2に長径10cm大の腫瘤影(b,c),両肺野に多発する小結節・結節影を認めた(d)。
臨床経過:入院後,原発性肺癌,肺炎・肺化膿症,肺結核,肺真菌症を鑑別に挙げ,確定診断のために気管攴鏡検査を施行した。右B2bより経気管支生検を施行したところ,病理組織のHematoxylin-eosin染色では腫瘍細胞は認めず,一部に壊死を伴う肉芽組織を認めた(図2a)。グロコット染色では黒色に染色される球状菌体を多数認め(図2b),気管支洗浄の培養にてC. neoformansが検出され肺クリプトコッカス症と診断した。また髄液の墨汁染色にて莢膜を有する球形真菌を認め,培養陽性よりクリプトコッカス髄膜炎と診断した。血清クリプトコッカス抗原は陽性であった。クリプトコッカス髄膜炎の標準治療はliposomal amphotericin B(L-AMB)+5-fluorocytosine(5-FC)であるが,本症例は93歳と超高齢であり,両剤の副作用が危惧されたため,VRCZによる治療を選択した。VRCZの投与量は初日1回300mg,1日2回,2日目以降1回200mg,1日2回食間に内服とした。投与開始7日目の血中トラフ濃度は1.5μg/mLと有効治療域であった。VRCZによる副作用は特に問題なく内服継続可能であり,治療開始後約2カ月後には肺野陰影は著明に縮小傾向し,症状も軽快し退院し外来治療に移行した。
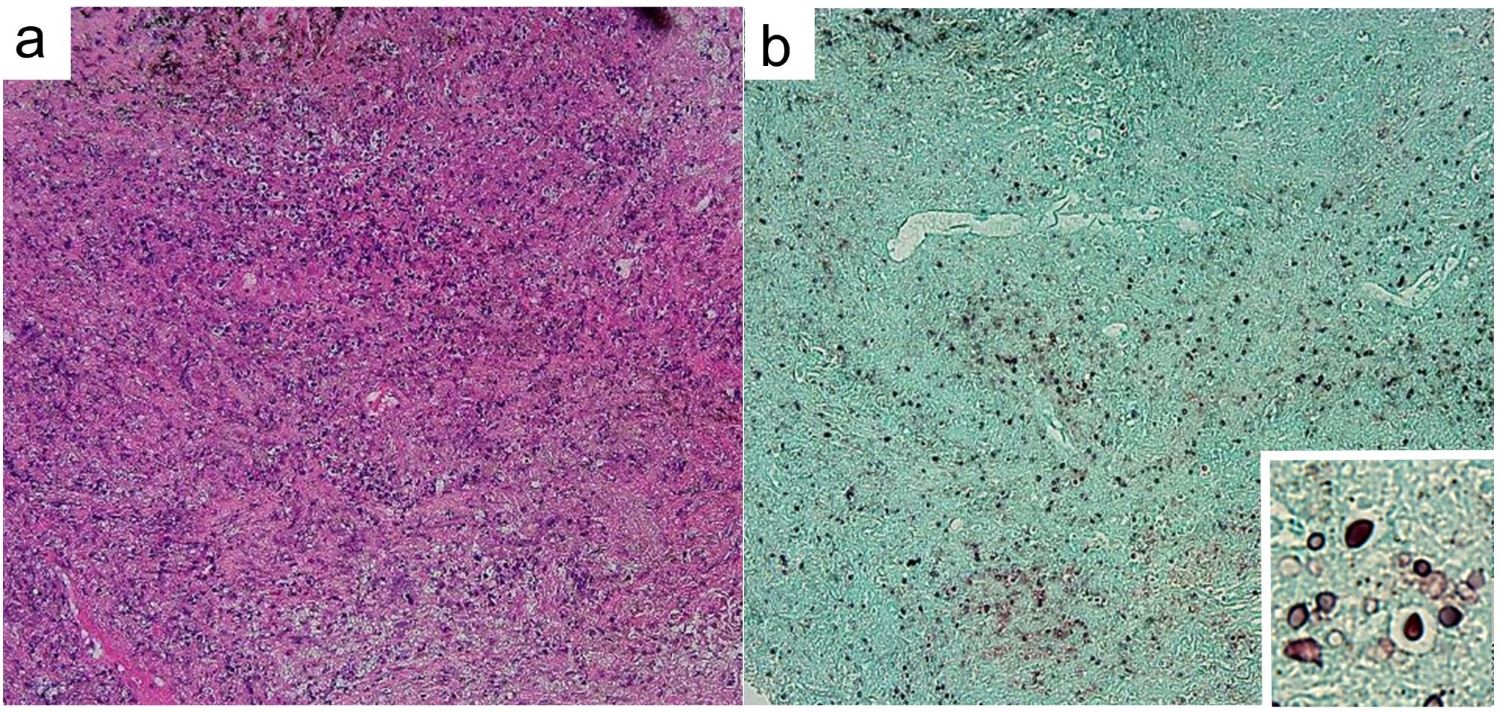 図2 経気管支生検の病理組織所見
図2 経気管支生検の病理組織所見 Hematoxylin-eosin染色(a,×100)では腫瘍細胞は認めず,一部に壊死を伴う肉芽組織を認めた。Grocott染色(b,×100)では黒色に染色される球状菌体を多数認めた。球状菌体の拡大像(inset,×400)。
クリプトコッカス症の起炎菌は日本ではほぼC. neoformansであり,肺と中枢神経に親和性がある。経気道感染後に肺病変および髄膜炎をきたしやすく,HIV感染などの基礎疾患を持たない健常者においても髄膜炎は稀ではない[5]。クリプトコッカス症は基礎疾患の認められない健常者に発症する原発性と,HIV,糖尿病患者などに日和見感染症として発症する続発性とに分類される。一般に原発性では単発性ないし多発性結節影を呈し[6],続発性では浸潤影や胸水貯留など多彩な画像を呈すると言われている[7]。芦沢らの報告では,結節・腫瘤を主体とするものが90%(孤発性30%,多発性60%),浸潤影主体(粒状影・結節・腫瘤も混在含む)が10%とされる。結節・腫瘤の大きさは5~75mmであり,肺癌,肺結核,時に細菌性肺炎などとの鑑別が問題になると報告されている[8]。岸らの報告では2cm大以下の病変が83%を占めていた[9]。Zhangらの報告では76人中7人に5cm超の孤立性結節を認めたとされている[10]。巨大腫瘤影を呈する肺クリプトコッカス症は過去に報告されているが,必ずしも免疫不全を合併していない[11][12][13]。本症例は超高齢者においてリウマチ性多発筋痛症に対するステロイド内服中および糖尿病治療中に発症した続発性クリプトコッカス症であり,長径10cm大の巨大腫瘤影,多発結節影など多彩な肺野病変を呈した。
肺クリプトコッカス症における外科手術の適応は,抗真菌薬が無効な例,肺癌を否定できない例などに限られ,基本的には薬物療法が主体である[14]。2019年の日本のガイドラインでは,本症例のような免疫不全者におけるクリプトコッカス髄膜炎や播種性クリプトコッカス症に対しては,induction therapyとしてL-AMB+5-FCを少なくとも2週間かつ髄液培養陰性までの投与およびconsolidation therapyとしてfluconazole(FLCZ)点滴あるいは内服を8週間投与,maintenance therapyとしてFLCZ内服を6~12カ月投与が第一選択として推奨されている。しかしinduction therapyとしてL-AMBおよび5-FCが使用困難な場合はVRCZの使用が推奨されている。その場合,VRCZはinduction therapyとして少なくとも2週間かつ髄液培養陰性までのVRCZの点滴投与,その後consolidation therapyとしてVRCZ内服を8週間投与,maintenance therapyとしてVRCZ内服を6~12カ月投与が示されている[15]。
L-AMBによる腎障害,5-FCによる胃腸障害や骨髄毒性には注意が必要であり,特に腎障害を有する者,低体重,高齢者では血中濃度が高くなり副作用が強く出ることがある。本症例では93歳と超高齢でありL-AMBおよび5-FCは副作用が危惧されたことから使用を避け,VRCZ内服による治療を選択した。VRCZは安定した高い吸収率や組織移行性が良好であり,経口・注射両方の剤形があり,長期治療が必要な真菌症の治療において極めて有用である。さらにtherapeutic drug monitoring(TDM)を行い,有効性・安全性を高める目的で血中濃度測定結果による用量調節が推奨されている。VRCZの血中濃度のトラフ値は有効性の面から1~2μg/mL以上を目標とし,肝障害などの副作用を避けるためには4~5μg/mL以下とすることが推奨される。本症例においてもTDMを行い安全に長期間の治療を行うことができ,巨大クリプトコッカス肺病変に対しても有効であった。
利益相反:開示すべき利益相反はない。
The patient was a 93-year-old female receiving oral steroids for polymyalgia rheumatica and undergoing treatment for diabetes mellitus. She was admitted to our hospital for fever, cough, and disturbance in her level of consciousness. Chest computed tomography revealed a giant mass of 10 cm in length in the right upper lobe and multiple nodular shadows in the bilateral lung fields. Based on bronchoscopy-guided transbronchial lung biopsy of the mass in the right upper, pulmonary cryptococcosis was diagnosed. As the patient had concomitant meningitis, treatment with voriconazole was initiated, and her symptoms gradually improved. Long-term treatment was possible with no significant adverse events.

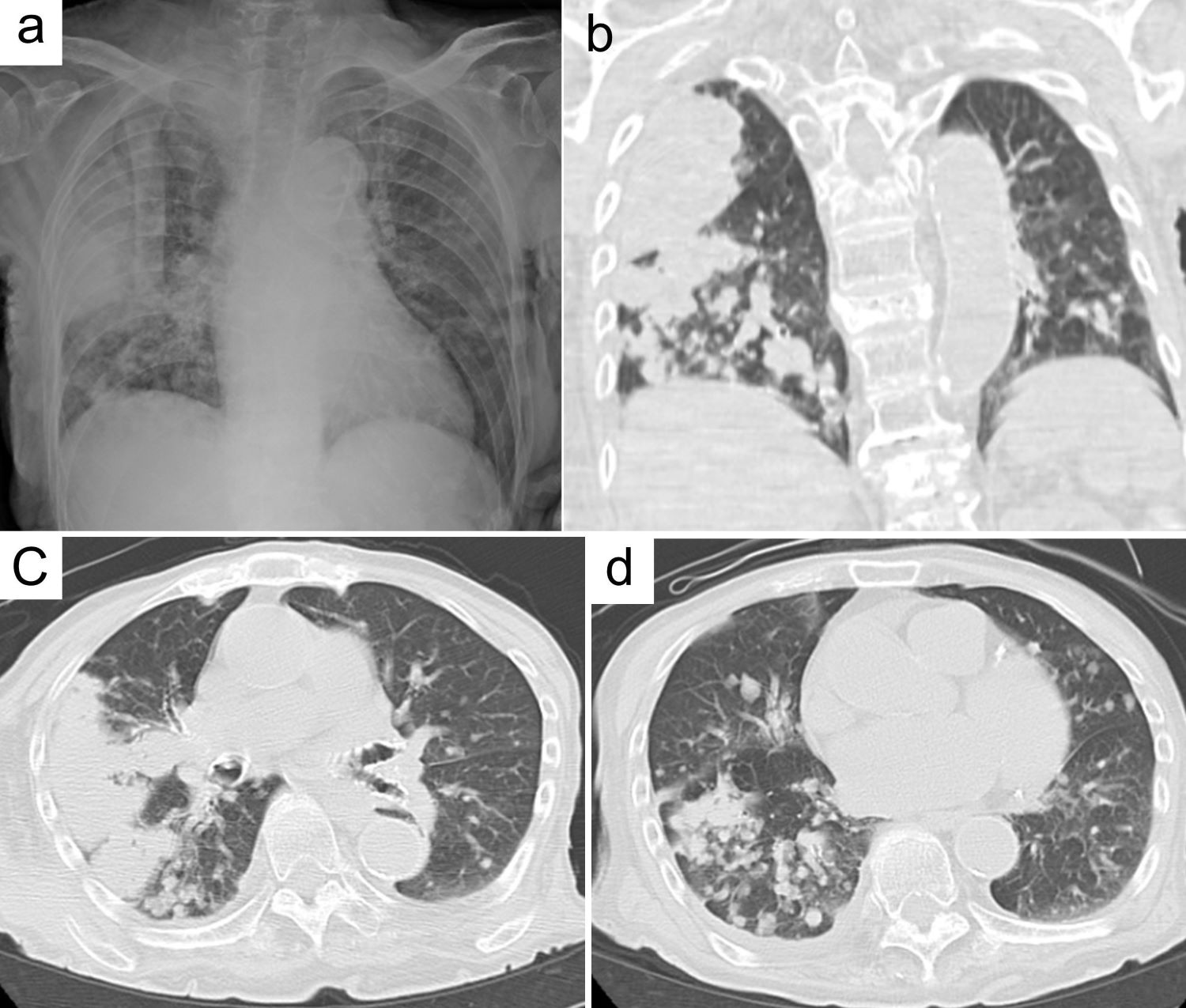
 図2 経気管支生検の病理組織所見
図2 経気管支生検の病理組織所見