長尾喬生*1,*2,横尾慶紀*1,菅谷文子*1,竹中 遙*1,関川元基*1,Ivor Cammack*3,山田 玄*1
*1手稲渓仁会病院呼吸器内科(〒006-0811 北海道札幌市手稲区前田1条12-1-40)
*2市立釧路総合病院呼吸器内科
*3手稲渓仁会病院臨床研修部
A case of IgG4-related respiratory disease diagnosed by endobronchial ultrasound-guided transbronchial needle aspiration
Takayuki Nagao*1,*2, Keiki Yokoo*1, Fumiko Sugaya*1, Haruka Takenaka*1, Motoki Sekikawa*1, Ivor Cammack*3, Gen Yamada*1
*1Department of Respiratory Medicine, Teine Keijinkai Hospital, Hokkaido
*2Department of Respiratory Medicine, Municipal Kushiro General Hospital, Hokkaido
*3Department of Clinical Residency, Teine Keijinkai Hospital, Hokkaido
Keywords:後腹膜線維症,リンパ節腫大,ステロイド療法/retroperitoneal fibrosis, lymphadenopathy, steroid treatment
呼吸臨床 2019年3巻11号 論文No.e00092
Jpn Open J Respir Med 2019 Vol. 3 No. 11 Article No.e00092
DOI: 10.24557/kokyurinsho.3.e00092
受付日:2019年8月20日
掲載日:2019年11月27日
©️Takayuki Nagao, et al. 本論文はクリエイティブ・コモンズ・ライセンスに準拠し,CC-BY-SA(原作者のクレジット[氏名,作品タイトルなど]を表示し,改変した場合には元の作品と同じCCライセンス[このライセンス]で公開することを主な条件に,営利目的での二次利用も許可されるCCライセンス)のライセンシングとなります。詳しくはクリエイティブ・コモンズ・ジャパンのサイト(https://creativecommons.jp/)をご覧ください。
患者:75歳,女性。
主訴:咳嗽。
既往歴:後腹膜線維症,高血圧症,脂質異常症。
生活歴:喫煙歴なし,アレルギーなし,粉塵吸入なし。
現病歴:72歳時に後腹膜線維症に伴う両側水腎症のため当院泌尿器科を受診した。同時に婦人科で子宮頸癌の診断となり,腹腔鏡下子宮および両側付属器摘除術となった。その時の免疫グロブリンはIgG 2,672mg/dl,IgG4 237mg/dlと上昇し,IgA 307mg/dl,IgM 69mg/dlと正常範囲内であったためIgG4関連疾患を疑い子宮頸癌手術の際に後腹膜生検を行った。しかし,病理学的検討では腹膜の線維性肥厚と巣状の単核球浸潤を認められたものの,花筵状線維化や閉塞性静脈炎は認められず,IgG4陽性形質細胞も2~3個/HPFと少数であったためIgG4-RDの診断には至らなかった。手術後に泌尿器科で水腎症の治療で約6カ月間のステロイド治療を施行されたが改善せず,対症的に尿管ステントが留置された。今回,治療3年後に約3カ月間持続する咳嗽と胸部異常陰影の出現のために当科に紹介となった。
身体所見:身長157cm,体重54kg,体温36.8℃,血圧107/50mmHg,脈拍86回/分整,SpO297%(室内気),眼瞼結膜に貧血なし,眼球結膜に黄染なし,涙腺・唾液腺の腫大なし,表在リンパ節の腫大なし,呼吸音清,心雑音なし,腹部異常所見なし,神経学的異常所見なし。
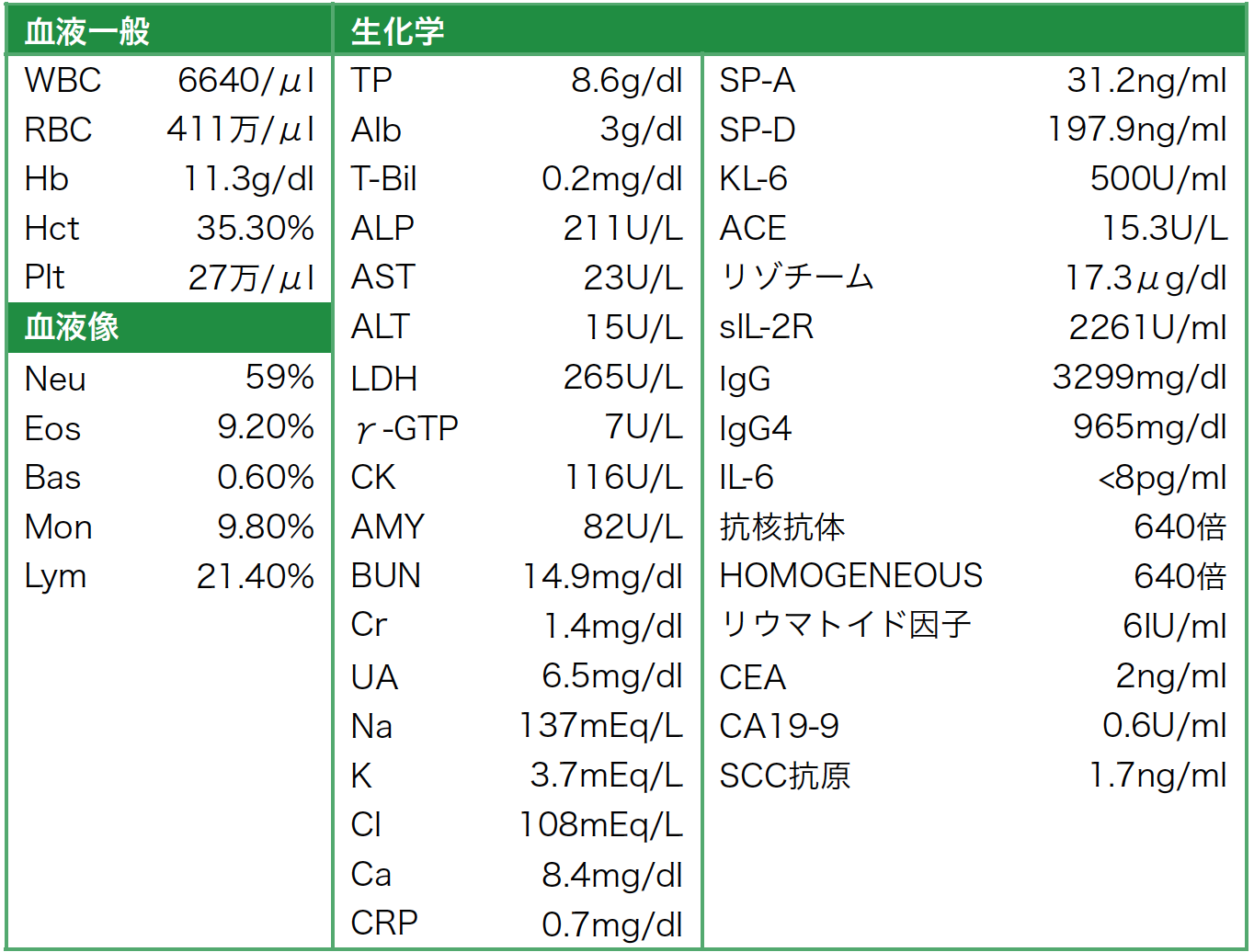
検査所見(表1):好酸球数と好酸球比率の軽度上昇,貧血,低アルブミン血症を認めた。IgG,IgG4,リゾチーム,可溶性IL-2受容体の上昇を認めた。なお,ACEとIL-6は正常範囲であり,抗核抗体は640倍・HOMO-GENEOUS640倍と高値であったが,自己抗体や腫瘍マーカーの上昇は認めなかった。
胸部X線像(図1):両側肺門リンパ節腫脹と右中肺野主体の粒状影を認めた。
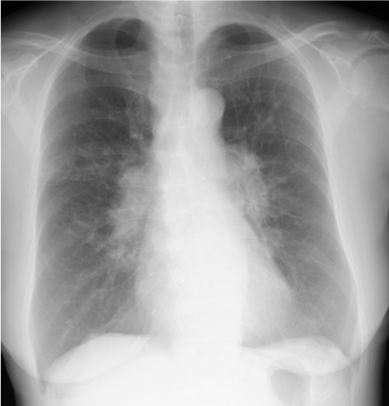
図1 胸部X線像
両側肺門リンパ節腫大と右中肺野に粒状影を認める。
胸部CT像(図2):右上葉(S2,S3)と左下葉(S6)を中心に分布する粒状影と気管支血管束の肥厚,縦隔リンパ節(#2R,#4R,#7)および肺門リンパ節の腫大を認めた。CT所見からはIgG4-RRD,多中心性Castleman病(MCD),サルコイドーシス,悪性リンパ腫などが鑑別疾患にあがった。
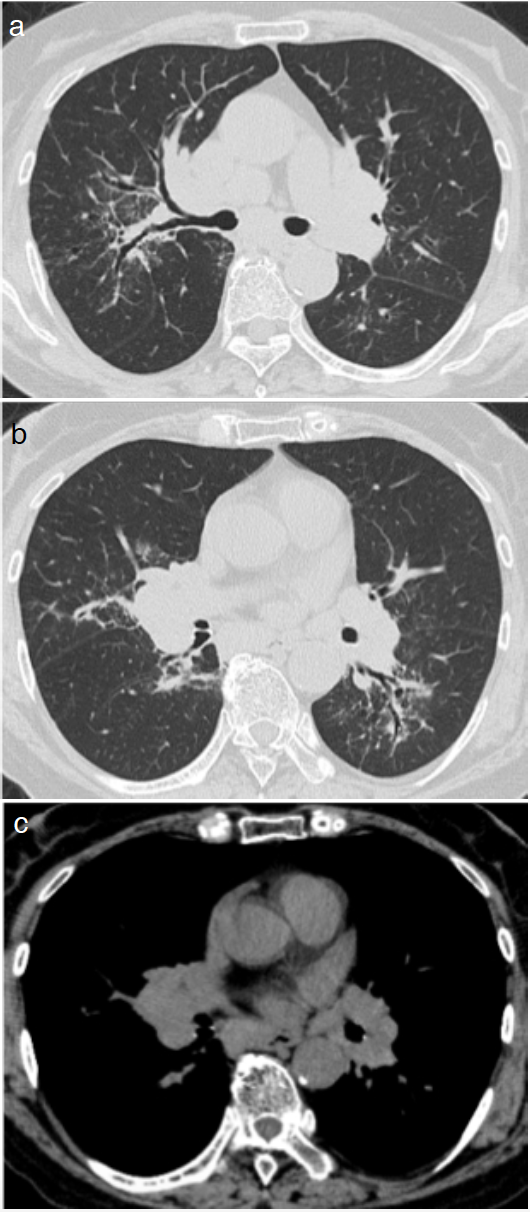
図2 胸部CT像
右上葉(S2,S3)と左下葉(S6)を中心に分布する粒状影と気管支血管束の肥厚,縦隔リンパ節(#2R,#4R,#7)および肺門リンパ節の腫大を認めた。
気管支鏡検査:気管支粘膜は全体的に発赤調かつ浮腫状であった。検査中は気管支鏡の挿入のみで容易に咳嗽が誘発され,気管支肺胞洗浄検査および経気管支肺生検は困難と判断し,気管分岐下リンパ節からEBUS-TBNAを施行した。
病理所見:生検組織では,多数のIgG4陽性形質細胞(20〜40個/HPF)を認め,IgG4/IgG陽性細胞比は高いところで80%だった。類上皮細胞性肉芽腫の形成や抗酸菌,真菌などの微生物は認めなかった(図3)。
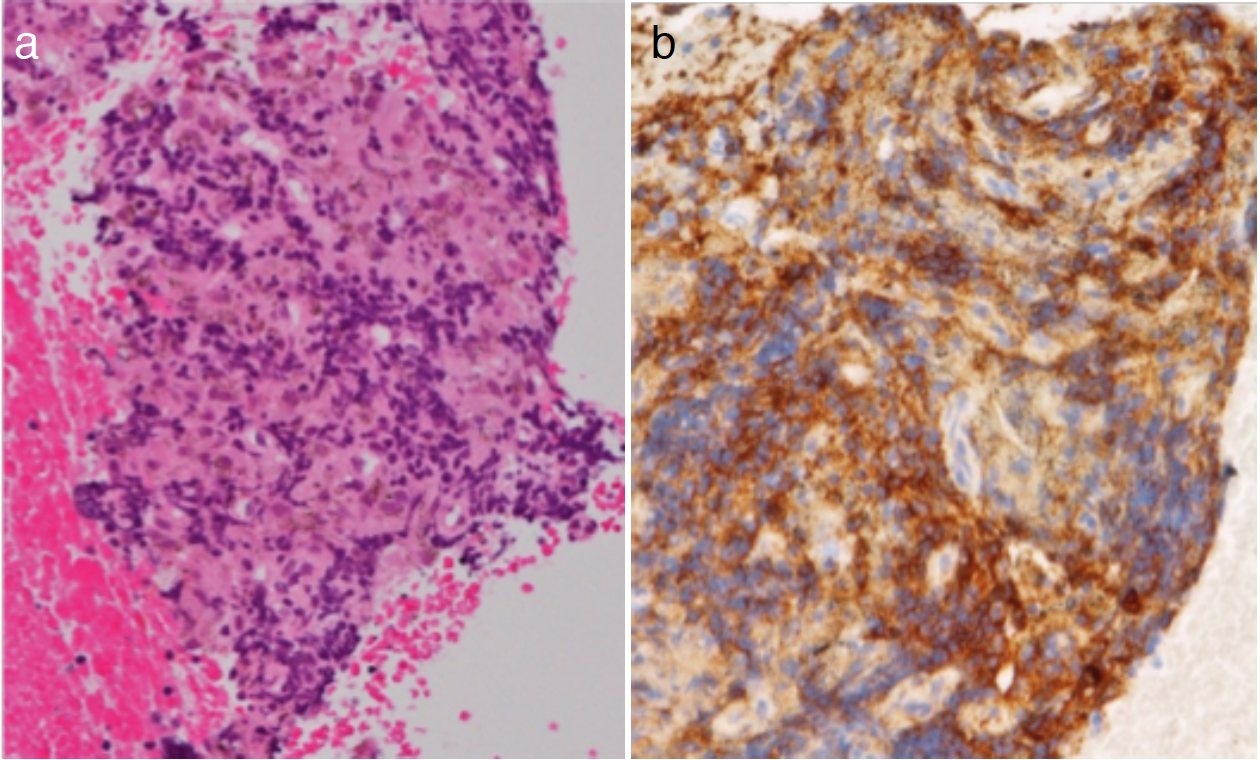
図3 気管分岐部リンパ節(#7)の生検組織
IgG4陽性形質細胞が20〜40個/HPF認められた(a. HE染色,X200,b. IgG4染色,X400)。
臨床経過:血清IgG4高値,組織検体でリンパ球,形質細胞の浸潤を認めたこと,IgG4/IgG陽性細胞比が80%程度かつIgG4陽性形質細胞が20〜40/HPFであったこと,および後腹膜線維症の合併を認めたことからIgG4-RRDと診断した。涙腺,唾液腺,膵臓,胆管などには明らかな病変を認めなかった。また,3年前のCTにおいても縦隔・肺門リンパ節の同程度の腫大を認めていたが肺野病変は認めなかった。本症例は症状が比較的軽度であり,自然軽快する症例[5]も報告されていることから経過観察を行った。しかし,診断1カ月後より咳嗽の悪化,呼吸困難も出現したため再入院とした。胸部CTでは肺病変の変化を認めなかったが,症状の増悪に対してステロイド療法を開始した。プレドニゾロン30mg/日(0.6mg/kg/日)を投与し,胸部CTで肺野病変の改善と縦隔リンパ節の縮小を認め,症状も改善した。プレドニゾロンは漸減し,6カ月間で投与を終了した。現在,経過観察中であるが再燃を認めていない。
2010年にFujinagaら[6]は,自己免疫性膵炎の患者90名の膵外病変を後方視的に分析し,肺門リンパ節腫大を78.3%に,肺病変を51.2%に認めたことを報告した。その後,Matsuiら[7]は,48例のIgG4-RRDの胸部CTの検討から肺門縦隔リンパ節腫大,気管支血管束の肥厚,小葉間隔壁肥厚,結節影,胸膜下や気管支壁周囲の浸潤影が特徴的な所見であることを明らかにした。IgG4-RRDの罹患臓器は全身諸臓器に及ぶが,肺においては広義間質であるリンパ路沿いを病変の場とする疾患と考えられ,胸部CTで本症を疑った場合は類似の所見を呈するサルコイドーシス,悪性リンパ腫,肺癌,MCDなどを鑑別する必要がある。本症例では気管支鏡挿入時の咳嗽のために経気管支肺生検が難しかったが,EBUS-TBNAで診断することができた。IgG4-RRDはほとんどの症例に縦隔リンパ節の腫大を合併するため[7],EBUS-TBNAによる縦隔リンパ節生検はIgG4-RRDの診断に有用と考えられる。
IgG4-RDは臨床症状が多彩であり,全身諸臓器に同時性または異時性に所見が出現する可能性がある。本症例は後腹膜線維症の治療3年後に胸郭内病変が増悪し,EBUS-TBNAで診断に至った。しかし,後腹膜線維症に対するステロイド療法では両側水腎症の改善は得られず,対症的に尿管ステントが留置された。一般的に血清IgG4が高値を呈する後腹膜線維症においてはステロイドの反応性は良好であるが,病変部にリンパ球浸潤が主体の炎症期ではなく,線維化を主体とした硬化期に至っている場合には効果が乏しいとされている[8][9]。子宮頸癌術前にPET/CTを撮影しているが,尿管周囲に活動性炎症を示す所見は認めなかった。したがって,本症例で施行された後腹膜生検で診断に至らなかった原因としては,病巣部がすでに硬化期であった可能性あるいは採取した組織自体が少なかったことが推測された。また,今回施行したステロイド治療で肺病変は改善したが,後腹膜病変の改善が得られなかったことは,同一疾患に基づく病態であっても治療までの期間やリンパ球浸潤の程度などによりステロイドに対する反応性が異なる可能性が示唆された。
本症の診断ではIgG4の上昇とIgG陽性形質細胞の組織浸潤が特徴であるが,これらの所見は他疾患でもみられることがあるため,一定の診断基準を満たさなければならない。しかし,MCD,関節リウマチなどの膠原病などでも本症の診断基準を満たす場合があり,注意すべきである[10][11]。特にIgG4-RRDと診断した症例が全身性の炎症所見を呈する場合やステロイドに反応しない場合はMCDの可能性がある[12][13]。さらにMCDとIgG4-RRDの合併した症例の報告[13]やMCDと診断後に自己免疫性膵炎を発症したとする報告[14]もあり,IgG4-RRDの診断が得られた後も長期の経過観察が重要である。
謝辞:本症例の病理所見につきましてご教示をいただきました手稲渓仁会病院病理診断科(現:東北大学大学院医学系研究科病態病理学分野助教)大森優子先生に深謝いたします。
利益相反:なし。