【投稿/症例報告】ベンラリズマブが効果的であった非結核性抗酸菌症を合併した
アレルギー性気管支肺アスペルギルス症の1例

西山佑樹*,齋藤 暁*,小屋俊之*,菊地利明*
*新潟大学大学院医歯学総合研究科,呼吸器感染症内科学分野
(〒951-8520 新潟県新潟市中央区旭町通1番町757)
A case of allergic bronchopulmonary aspergillosis with nontuberculous mycobacteriosis for which benralizumab was effective
Yuki Nishiyama*, Akira Saito*, Toshiyuki Koya*, Toshiaki Kikuchi*
*Department of Respiratory Medicine and Infectious Diseases, Niigata University Graduate School of Medical and Dental Sciences, Niigata
Keywords:ベンラリズマブ,非結核性抗酸菌症,アレルギー性気管支肺アスペルギルス症,気管支喘息/benralizumab, nontuberculous mycobacteriosis, allergic bronchopulmonary aspergillosis, bronchial asthma
呼吸臨床 2021年5巻10号 論文No.e00137
Jpn Open J Respir Med 2021 Vol. 5 No. 10 Article No.e00137
DOI: 10.24557/kokyurinsho.5.e00137
受付日:2021年5月21日
掲載日:2021年10月8日
©️Yuki Nishiyama, et al. 本論文はクリエイティブ・コモンズ・ライセンスに準拠し,CC-BY-SA(原作者のクレジット[氏名,作品タイトルなど]を表示し,改変した場合には元の作品と同じCCライセンス[このライセンス]で公開することを主な条件に,営利目的での二次利用も許可されるCCライセンス)のライセンシングとなります。詳しくはクリエイティブ・コモンズ・ジャパンのサイト(https://creativecommons.jp/)をご覧ください。
症例は66歳,女性。気管支喘息で吸入ステロイド/長時間作用型β刺激薬(inhaled corticosteroid/long-acting β-agonists:ICS/LABA)を使用していたが,病状のコントロールが不良であったため,当院を紹介受診した。アレルギー性気管支肺アスペルギルス症(allergic bronchopulmonary aspergillosis:ABPA)と診断されたが,画像所見および喀痰培養で
Mycobacterium abscessus(
M.abscessus)を検出したため,非結核性抗酸菌症合併と判断し,経口副腎皮質ステロイドの使用を回避した。好酸球増多を伴っていたことから,ベンラリズマブを導入された。導入後に喘息コントロールは改善し,入院時の胸部CT検査で認めた粘液栓は消退した。
ABPAは気道内に定着したアスペルギルス属真菌に対するⅠ型・Ⅲ型アレルギー反応の結果生じる疾患である。気道内に真菌が定着することで持続的なTh2,Th17免疫反応が誘導され,真菌特異的IgE,IgG産生が生じる[1]とともに,extracellular trap cell death(ETosis)を起こした好酸球から粘性の高いクロマチン線維が放出されて粘液栓が形成される[2][3]。ベンラリズマブは,好酸球の表面に発現するIL-5受容体に対し直接的に作用するヒト化抗IL-5受容体α鎖モノクローナル抗体製剤である。ベンラリズマブは,抗体依存性細胞傷害活性(ADCC活性)を高め,IL-5受容体を発現している好酸球を速やかかつほぼ完全に除去する特徴を持っている[4]。今回われわれは非結核性抗酸菌症(nontuberculous mycobacteriosis:NTM)を合併したABPAの症例にベンラリズマブが著効した1例を経験したので,文献的考察を加えて報告する。
主訴:呼吸困難感,咳嗽。
現病歴:気管支喘息の発症は3歳頃で,小中学生の時には発作が強く,救急外来を何度も受診した既往があった。高校生の頃に臨床的寛解状態となったが,30歳の時に妊娠を契機に喘息症状が再燃した。気管支喘息に対し中等量のフルチカゾンプロピオン酸エステル/ホルモテロールフマル酸塩水和物吸入治療を行っていたが,常に狭窄音を聴取し,呼吸機能検査では閉塞性換気障害が残存して,病状のコントロールは不良であった。また以前から画像所見よりNTMの疑いで経過観察されていた。前医で撮影された胸部CT検査でNTM感染を疑わせる小粒状影・線状影の他に,中枢気管支内の粘液栓を複数箇所認めた。精査・加療目的に当院を紹介受診した。
既往歴:64歳時に喀血し止血剤で治療。
既存症:Basedow病。
内服薬:ルパタジンフマル酸塩10mg/日,カルボシステイン1500mg/日,ミコナゾールゲル,レボチロキシンナトリウム水和物100µg/日。
吸入薬:フルチカゾンプロピオン酸エステル/ホルモテロールフマル酸塩水和物吸入剤125エアゾール,1日2回,1回2吸入。長時間作用型抗コリン薬は気分不快があり使用できず。
職業歴:事務職(トレーニングセンター受付)。
環境情報:ガーデニングや畑仕事など,土いじりが多い環境はない。
喫煙歴:なし。
アレルギー歴:小児喘息,アトピー性皮膚炎(無治療),通年性アレルギー性鼻炎。
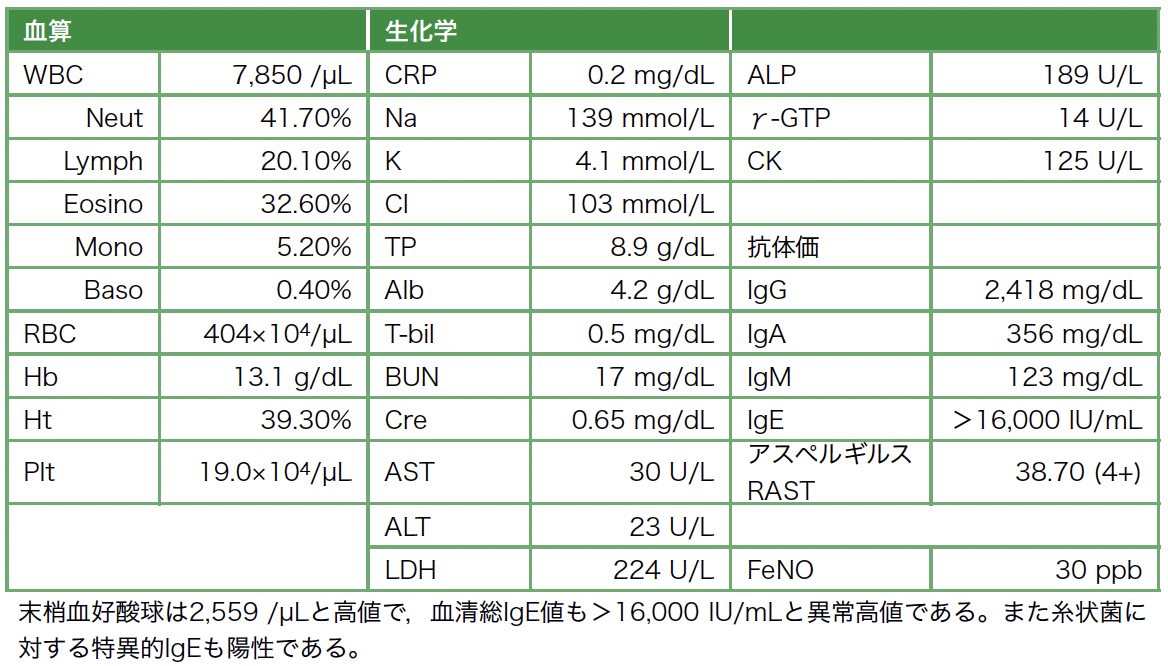
初診時現症:身長158cm,体重46.0kg,BMI 18.42kg/m2,体温36.5℃,血圧110/66mmHg,呼吸回数14/min,脈拍80/min・整,SpO2 97%(室内気)。意識清明,表在リンパ節の腫脹なし。胸部;心音正常。呼吸音:呼気終末にwheezesを聴取,腹部;平坦で軟,圧痛なし。四肢;浮腫なし(表1,図1)。
表1 初診時血液学的検査所見
図1 Aspergillus fumigatusに対する沈降抗体反応
すべての抗原ウェルと患者血清ウェルの間に沈降線が見られ,強陽性を示している。
Pt:Patient’s serum,PC:Positive Control,NC:Negative control,CF:Aspergillus fumigatus culture filtrate antigens,SOM:Aspergillus fumigatus somatic antigens
喀痰一般細菌検査:Pseudomonas alcaligenes 2+,Aspergillus spp 1+。
喀痰抗酸菌検査:M.avium,M.intracellulareはともにPCR陰性であった。液体培養でM.abscessusを検出した(図2,3)。
心電図検査:HR 88bpm,正常範囲。
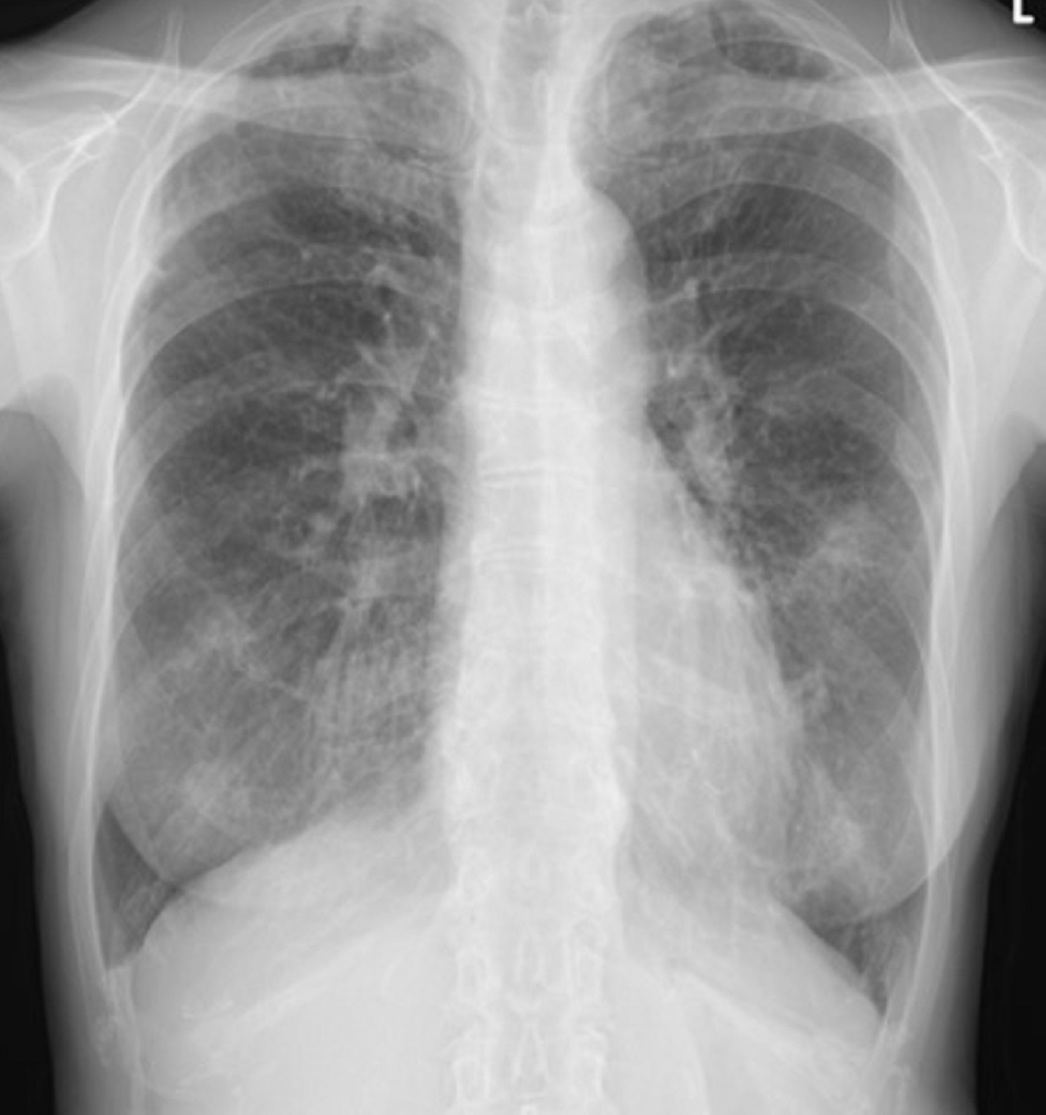
図2 初診時胸部X線写真
両肺野に結節影が多発している。
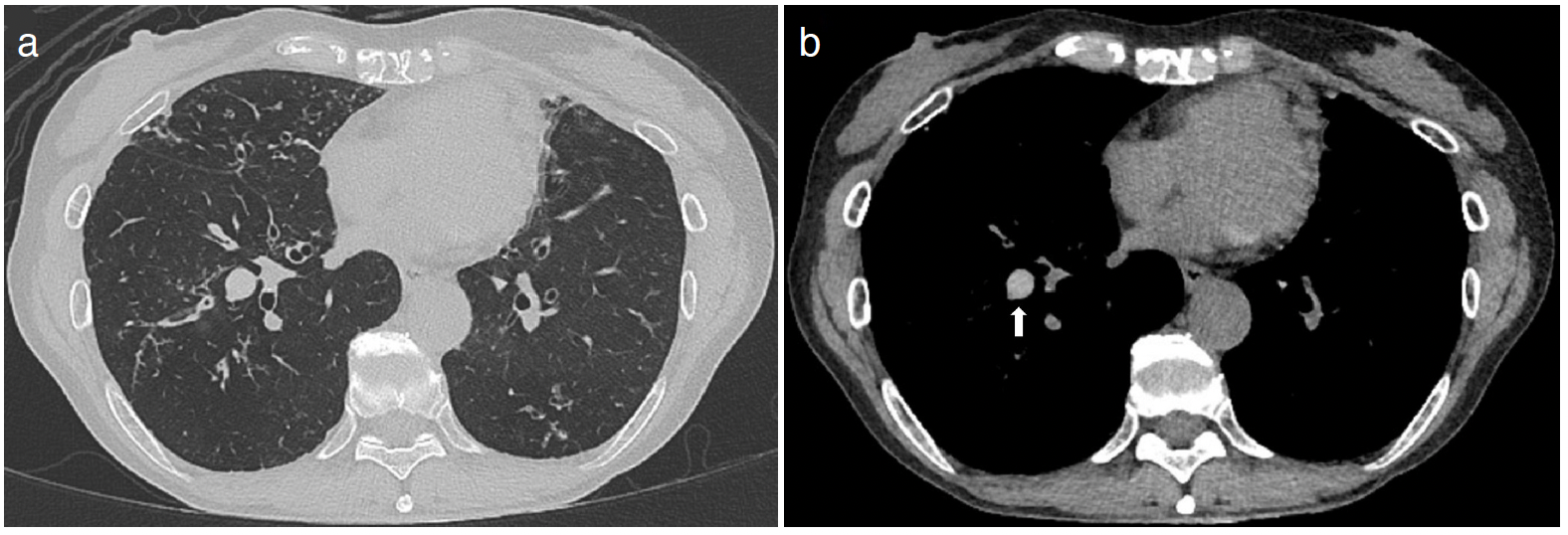
図3 初診時胸部CT写真(a. 肺野条件,b. 縦郭条件)
右下葉中枢気管支内に粘液栓を認める。粘液栓は縦隔条件で濃度上昇(high-attenuation mucus:HAM)を伴っている(矢印)。右中葉主体に粒状影,線状影や気管支拡張症に伴う慢性気道炎症の所見がある。
本症例は初診時検査所見で,①喘息症状あり,②末梢血好酸球(ピーク時)≧500/mm3,③血清総IgE値(ピーク時)≧417 IU/mL,④糸状菌に対する特異的IgE陽性,⑤糸状菌に対する沈降抗体陽性,⑥喀痰で糸状菌培養陽性,⑦胸部CT検査で中枢気管支内粘液栓があり,⑧粘液栓は縦隔条件で濃度上昇(HAM)を認め,アレルギー性気管支肺真菌症の診断基準(「アレルギー性気管支肺真菌症」研究班)の10項目中8項目に当てはまり,診断基準である6項目以上を満たしたことから,ABPAと診断した。またそれと同時期の喀痰培養でM.abscessusを検出した。確定診断目的に気管支内視鏡の施行を提示したが,希望されなかった。M.abscessusはコンタミネーションが少ないこと,また画像所見が肺NTM症に矛盾しないことから,M.abscessusによる肺NTM症合併例であると判断した。さらに本症例において臨床症状と画像変化の主病態はABPAであると考え,治療の優先順位はABPAの方が高いと判断した。ABPAの標準治療は経口副腎皮質ステロイド薬の全身投与であるが,M.abscessusによる肺NTM症の合併症例であると判断したことから,経口副腎皮質ステロイドの使用は回避する方針とした。好酸球増多を伴っていたことから,ベンラリズマブを導入する方針とした。ベンラリズマブ開始後,末梢血および喀痰中好酸球数はゼロとなった。初診時に18点であった喘息コントロールテスト(The asthma control test:ACT)スコアは4カ月後には23点まで上がり,1年後も24点と良好なコントロールが維持されていた。喘息QOL質問票(Asthma Quality of Life Questionnaire:AQLQ)スコアも初診時は平均4.9点であったが,4カ月後には平均5.8点まで改善していた。そして胸部CT(図4)では中枢気管支内粘液栓の消退を確認した(表2)。
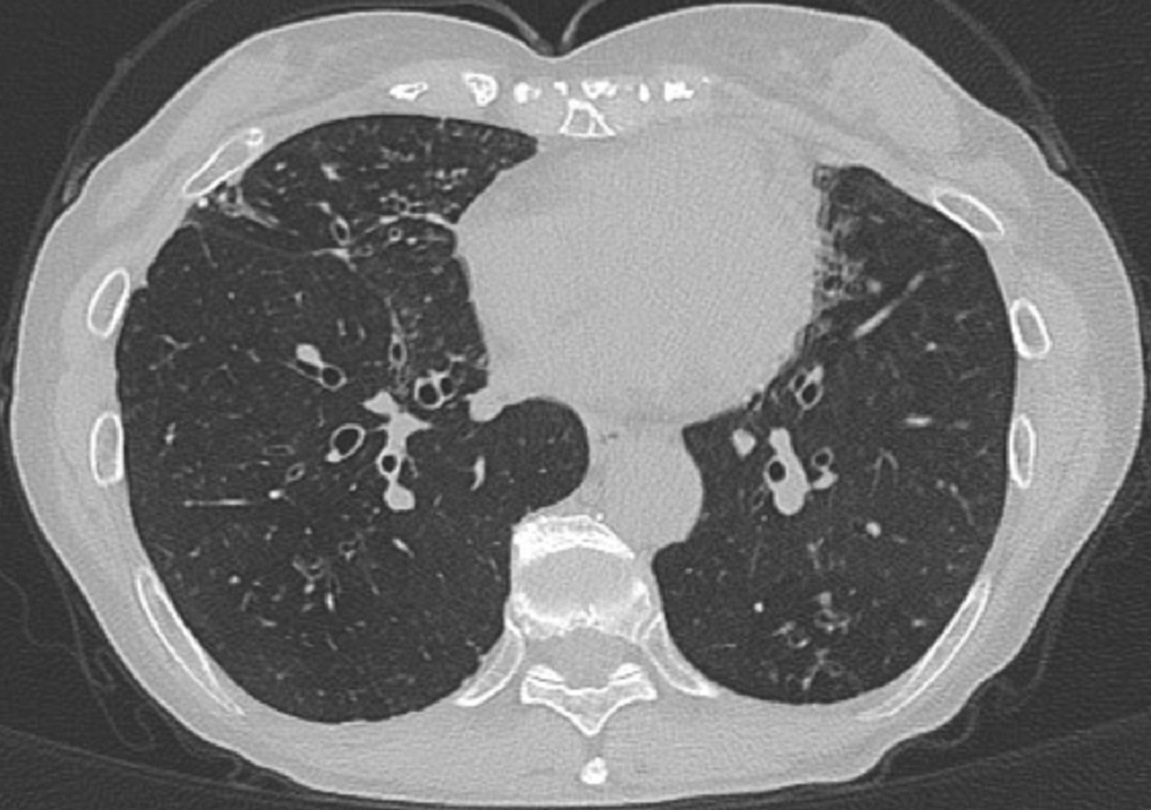
図4 治療後胸部CT写真
右下葉中枢気管支内の粘液栓は消退している。
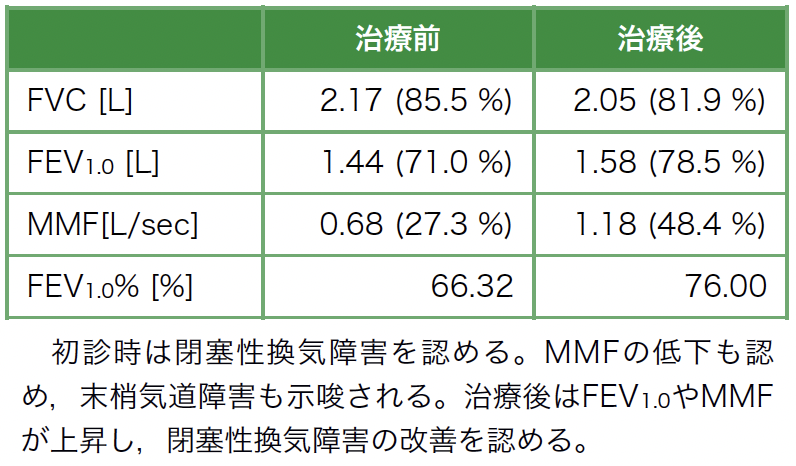
表2 治療前後呼吸機能検査
NTMはMycobacterium avium complex(MAC)が大部分を占めるが,M.abscessusは近年独立菌種として認められた稀少菌種である[5]。病変分布は早期から肺MAC症より全肺野広範囲な傾向が指摘されている[6]上,肺感染症として成立すると菌の根絶はMACよりはるかに困難,かつ治療後に再排菌を繰り返す例も報告されており,肺NTM症の中では最も難治と言われている。本症例では細菌学的に確定はされていなかったが,M.abscessusによる肺NTM症合併症例と判断して対応した。治療法を決定するに当たり,ABPAへの全身性ステロイドがNTM感染症を増悪させる可能性[7]やM.abscessus感染のリスクファクターであることを示唆する報告[8]や,肺NTM症などの慢性気道感染症を合併したABPAに対してオマリズマブの使用が安全性と有効性を示した報告[9]がみられたことから,本症例はABPAの標準治療である経口副腎皮質ステロイド薬ではなく,分子標的薬が検討された。分子標的薬を追加するに当たり,気管支喘息の治療として吸入ステロイドはまだ増量の余地があった。しかし以前より画像所見で肺NTM症の関与が疑われていたことから,高用量にしづらい状況にあった。また長時間作用型抗コリン薬も副作用のため継続使用ができず,症状コントロールのため,分子標的薬の使用に踏み切った。本症例はアトピー性皮膚炎を合併していたことから,IL-4受容体α鎖抗体(デュピルマブ)の使用も検討された。しかし血中好酸球数が高値であったことから,好酸球をターゲットにした治療がより有効であろうと考えた。ABPAにベンラリズマブが効果的であった症例報告もあり[10],本症例では同剤を選択した。ベンラリズマブによって好酸球を速やかかつほぼ完全に除去することで,気道過敏性や気道リモデリング等の喘息病態を阻害するとともに,ABPAの特徴の1つである粘液栓形成の原因である好酸球のETosisを回避することで,ABPAの改善に寄与したと考えられる。
利益相反:本主題に関して利益相反はない。
To treat allergic bronchopulmonary aspergillosis (ABPA), oral corticosteroids are commonly used. Here, we report a case of ABPA with nontuberculous mycobacterial infection (NTM), that is dramatically effective with benralizumab. A 66-year-old woman was mainly treated with inhaled corticosteroids / long-acting β-agonist for bronchial asthma. Her asthma condition was poorly controlled despite of therapy, and she was referred to our hospital. This case was diagnosed with ABPA, because peripheral blood eosinophilia, high total serum IgE, positive specific IgE and precipitated antibody for filamentous fungi, positive culture of filamentous fungus in sputum, central bronchial mucus plug on chest CT examination, and increased mucus plug concentration (high-attenuation mucus: HAM) were observed. However, she did not receive oral corticosteroids due to the comorbidity of NTM. Because of eosinophilia, benralizumab was introduced. One year after the introduction of benralizumab, the asthma control test (ACT) and the asthma quality of life questionnaire (AQLQ) score were improved. Chest CT examination showed the disappearance of the mucus plug in the central bronchus.
- 日本アレルギー学会/日本呼吸器学会, 監修. アレルギー性気管支肺真菌症の診療の手引き. 東京:医学書院, 2019.
- Ueki S, et al. Eosinophil extracellular trap cell death-derived DNA traps: Their presence in secretions and functional attributes. J Allergy Clin Immunol. 2016; 137: 258-67.
- Muniz VS, et al. Eosinophils release extracellular DNA traps in response to Aspergillus fumigatus. J Allergy Clin Immunol. 2018; 141: 571-85.
- J Mark FitzGerald, et al. Benralizumab, an anti-interleukin-5 receptor α monoclonal antibody, as add-on treatment for patients with severe, uncontrolled, eosinophilic asthma (CALIMA): a randomized, double-blind, placebo-controlled phase 3 trial. Lancet. 2016; 388: 2128-41.
- Kusunoki S, et al. Application of colorimetric microdilution plate hybridization for rapid genetic identification of 22 Mycobacterium species. J Clin Microbiol. 1991; 29: 1596-603.
- Han D, et al. Radiographic and CT findings of nontuberculous mycobacterial pulmonary infection caused by Mycobacterium abscessus. AJR. 2003; 181: 513-7.
- Ishiguro T, et al. Pulmonary nontuberculous mycobacteriosis and chronic lower respiratory tract infections in patients with allergic bronchopulmonary mycosis without cystic fibrosis. Intern Med. 2016; 55: 1067-70.
- Mussaffi H, et al. Nontuberculous mycobacteria in cystic fibrosis associated with allergic bronchopulmonary aspergillosis and steroid therapy. Eur Respir J. 2005; 25: 324-8.
- Tomomatsu K, et al. Effectiveness and safety of omalizumab in patients with allergic bronchopulmonary aspergillosis complicated by chronic bacterial infection in the airways. Int Arch Allergy Immuno. 2020; 181: 499-506.
- Matsuura H, et al. Successful treatment with benralizumab for allergic bronchopulmonary aspergillosis that developed after disastrous heavy rainfall in western Japan. Intern Med. 2021; 60: 1443-50.