中村和憲*1,西山健太*1,関戸祐子*1,仁田脇辰哉*1,飯尾美和*1,久永純平*1,坂田能彦*1,神宮直樹*1,江口善友*1,保田祐子*1,川村宏大*1,村中裕之*1,中村悠太*2,中山雄二朗*2,鵜木 崇*3,澤村匡史*3,一門和哉*1
*1済生会熊本病院呼吸器科(〒861-4193 熊本県熊本市南区近見5-3-1)
*2同 救急・総合診療科,*3同 集中治療室
A severe case of novel coronavirus-associated pneumonia ; avoiding tracheotomy and withdrawal from long-term artificial ventilation management
Kazunori Nakamura*1, Kenta Nishiyama*1, Yuko Sekido*1, Tatsuya Nitawaki*1, Miwa Iio*1, Jumpei Hisanaga*1, Yoshihiko Sakata*1, Naoki Shingu*1, Yoshitomo Eguchi*1, Yuko Yasuda*1, Kodai Kawamura*1, Hiroyuki Muranaka*1, Yuta Nakamura*2, Yujiro Nakayama*2, Takashi Unoki*3, Tadashi Sawamura*3, Kazuya Ichikado*1
*1Division of Respiratory, *2Department of Acute Care & General Medicine, *3Department of Intensive Care Unit, Saiseikai Kumamoto Hospital, Kumamoto
Keywords:新型コロナウイルス感染症,COVID-19,人工呼吸管理,ファビピラビル,ナファモスタットメシル/severe acute respiratory syndrome coronavirus-2(SARS-CoV-2),coronavirus infectious disease 2019(COVID-19),mechanical ventilation,favipiravir,nafamostat mesylate
呼吸臨床 2020年4巻11号 論文No. e00112
Jpn Open J Respir Med 2020 Vol. 4 No. 11 Article No.e00112
DOI: 10.24557/kokyurinsho.4.e00112
受付日:2020年8月31日
掲載日:2020年11月27日
©️Kazunori Nakamura, et al. 本論文はクリエイティブ・コモンズ・ライセンスに準拠し,CC-BY-SA(原作者のクレジット[氏名,作品タイトルなど]を表示し,改変した場合には元の作品と同じCCライセンス[このライセンス]で公開することを主な条件に,営利目的での二次利用も許可されるCCライセンス)のライセンシングとなります。詳しくはクリエイティブ・コモンズ・ジャパンのサイト(https://creativecommons.jp/)をご覧ください。
現病歴:66歳男性。X−9日より発熱が出現,X−3日意識が遠のくようなめまい症状を自覚し近医救急外来を受診した。38.7℃の発熱を伴い,胸部CTで両肺にびまん性のすりガラス状陰影を認め同院へ入院した。X−2日喀痰・咽頭ぬぐい液で核酸増幅検査を施行し,SARS-CoV-2(severe acute respiratory syndrome coronavirus-2)陽性となった。X−1日に感染症指定病院へ転院搬送となり,シクレソニド吸入800μg/日,ファビピラビル3,600mg/日,アジスロマイシン(AZM)500mg/日を開始された。当初は室内気でSpO2 95%程度を維持できていたが,酸素化が悪化傾向となり,X日午前には経鼻カニューレで酸素5L/分を要したため,集中治療目的に当院へ転院となった.
既往歴:2型糖尿病(51歳),睡眠時無呼吸症候群(発症時期不詳),右大腿骨骨折(27歳),白内障(64歳)。
常用薬:メトホルミン。
嗜好歴:50本/日×30年間の喫煙歴,50歳時に禁煙した。ビール350mL/日の飲酒あり。
職業歴:タクシー運転手。
生活歴:渡航歴なし。COVID-19患者や有熱者との明らかな接触歴はなく,活動は自宅と職場の往復程度。
入院時現症:咳嗽・喀痰あり,味覚・嗅覚障害なし。身長167cm,体重77.70kg。意識清明。血圧162/90mmHg,心拍数88回/分,呼吸数24回/分,体温36.7℃,SpO2 96%(経鼻カニューレ酸素5L/分)。
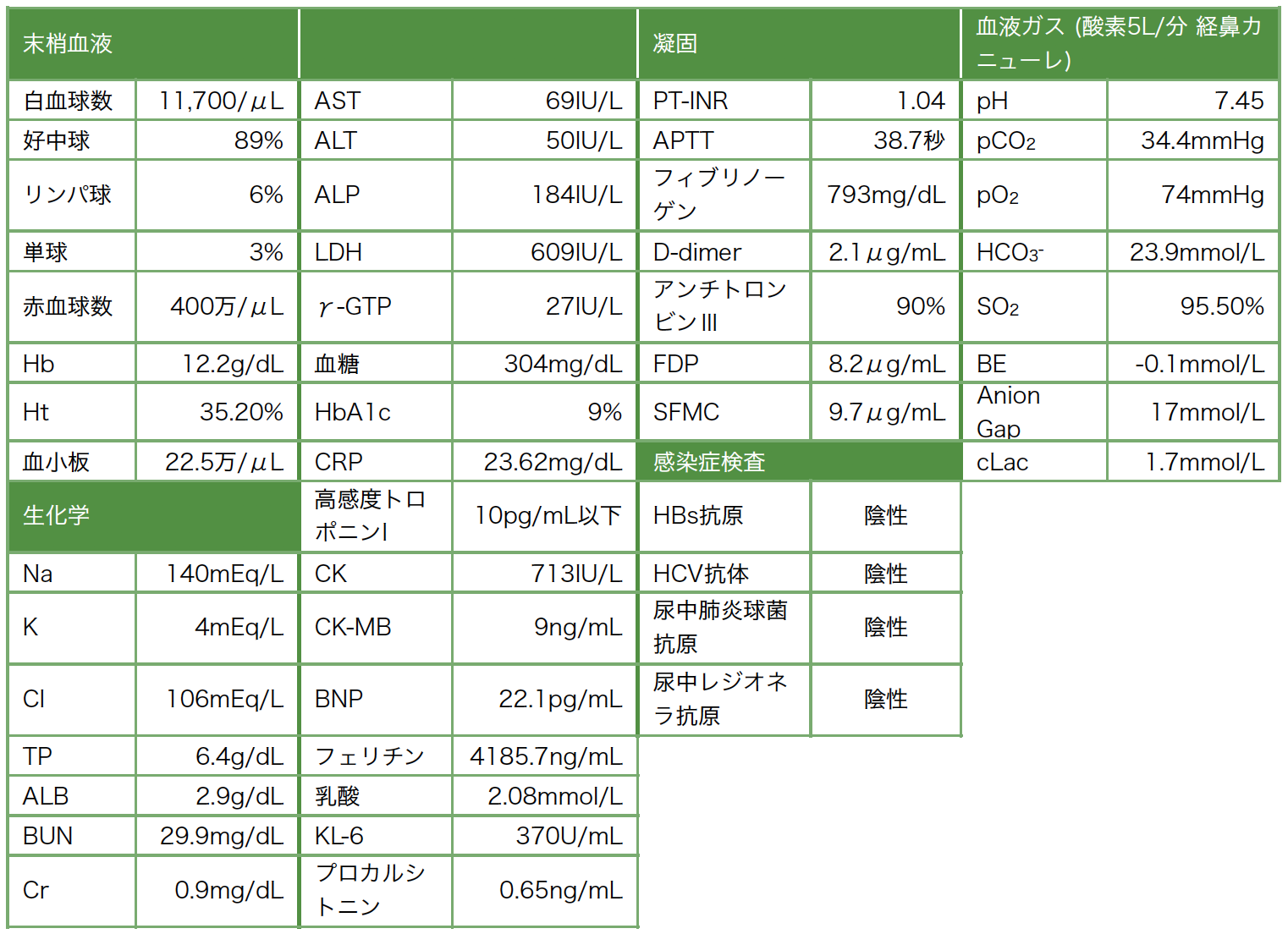
入院時検査所見:末梢血;白血球11,700/μL(リンパ球6.0%,好中球89%),C反応性蛋白(CRP)23.62mg/dL,フェリチン4185.7ng/mL。血小板数は22.5万/μL,D-dimer 2.1μg/mL,FDP 8.2μg/mL,フィブリノーゲン793mg/dL。血糖304mg/dL,HbA1c 9.0%。
動脈血ガス分析:経鼻カニューレ酸素5L/分吸入下にPaO2 74.0Torr(表1)。
表1 入院時検査所見
胸部X線写真:両肺の胸膜直下にすりガラス状陰影を認める(図1)。
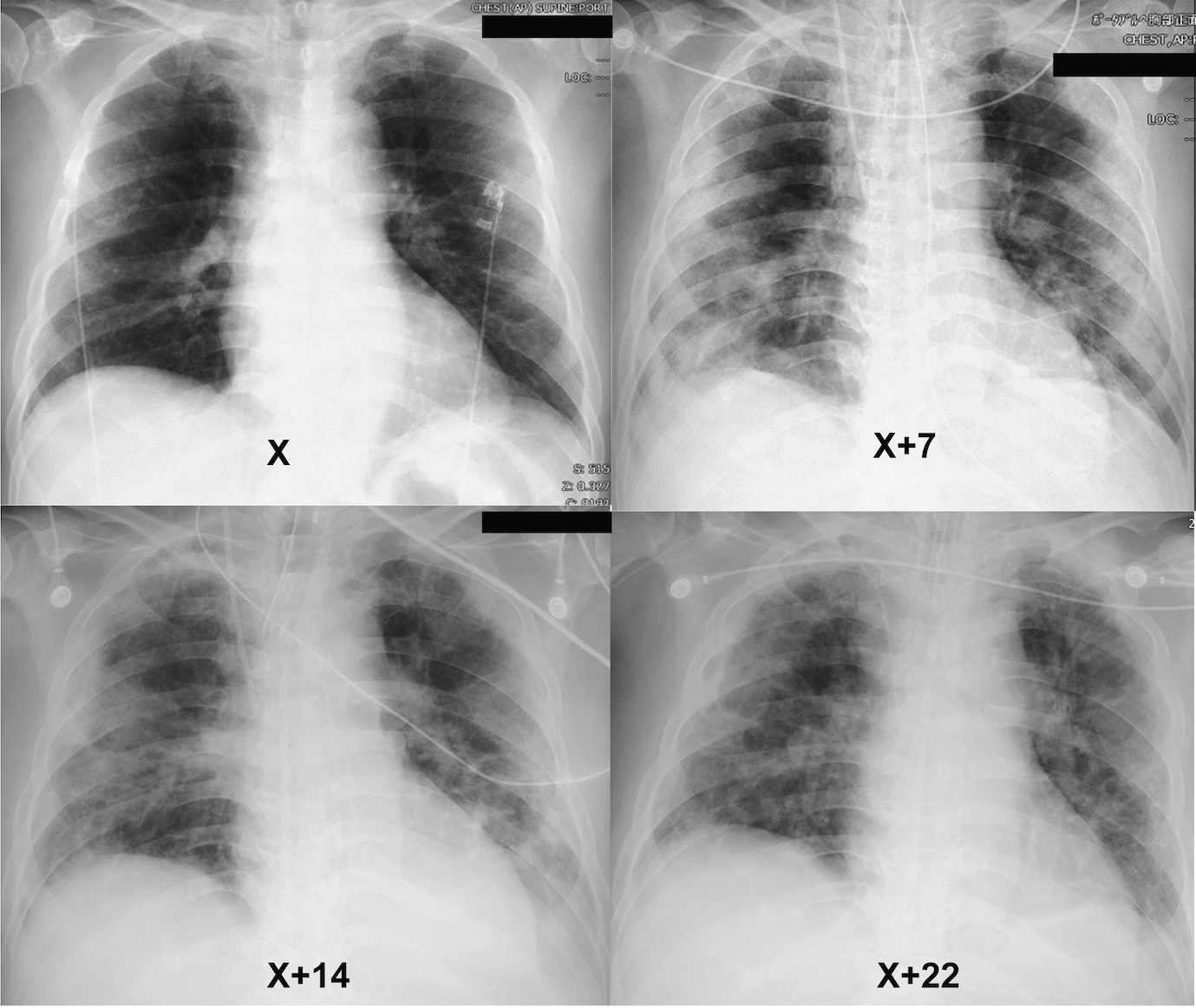
図1 胸部X線画像
両肺のすりガラス状陰影の経時的な拡大を認めた。
CT所見:X−3日に撮像。背景に気腫性変化があり,両側胸膜下・末梢優位にすりガラス状陰影を認める(図2)。
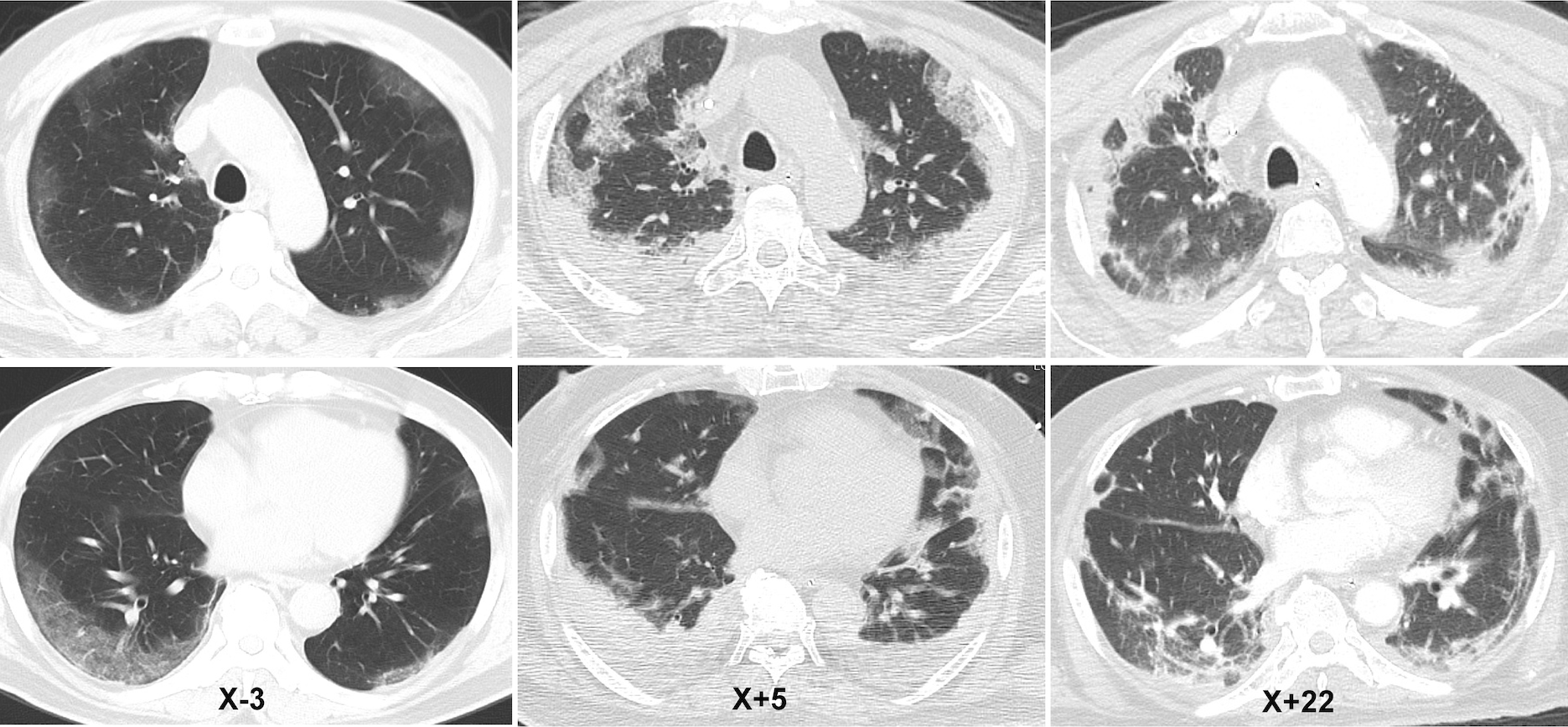
図2 胸部CT画像
発症初期ではすりガラス状陰影であったが,病勢の進行に伴い胸膜直下の浸潤影が主体となった。呼吸不全の改善に伴い,浸潤影は消退傾向となった。
臨床経過:酸素需要量の急速な増加のため,当院転院後挿管人工呼吸管理となった。挿管後のPaO2/FIO2比(P/F比)は187と中等症の急性呼吸窮迫症候群(acute respiratory distress syndrome:ARDS)(Berlin定義)であった。入院当日よりファビピラビル(X日より1,600mg/日),AZMを継続した。D-dimer高値のため抗凝固目的にX+1日よりナファモスタットの併用を開始した。酸素化の改善に乏しく,炎症反応及びフェリチン高値が遷延しており,X+3日よりメチルプレドニゾロン(mPSL)40mg/日の投与を開始,細菌性肺炎の併発が懸念されセフトリアキソン(CTRX)を開始した。X+4日より抗凝固療法をヘパリンに変更した。胸部CTを撮像したところ,以前のすりガラス状陰影は浸潤影に変化していた。閉鎖回路式人工呼吸管理ではあったが,体位変換時に回路が外れ,病室内にエアロゾルの産生を来す懸念があった。そのためリハビリテーションでは,X+3日からのベッド上でのキッキング,X+7日からの体位変換・チェアポジションまでに控え,腹臥位療法は施行しなかった。X+11日から再発熱・粘稠痰の増加を認めた。細菌性肺炎の加療のため度重なる抗菌薬変更を必要としたが改善に乏しく,喀痰培養からStenotrophomonas maltophiliaが検出され,感受性良好な抗菌薬に変更後から解熱・臨床症状の改善が得られた。改善不良な肺炎については人工呼吸器との関連が否定できず,長期挿管に伴う喉頭浮腫・上気道閉塞のリスクもあり,気管切開を避ける必要性について議論がなされた。診療当時SARS-CoV-2の感染性が十分に判明していなかったことから,医療従事者への二次感染予防の目的で気管切開を可能な限り避けることになった。最終的にX+26日に抜管に至り,X+29日転院となった(図3,4)。
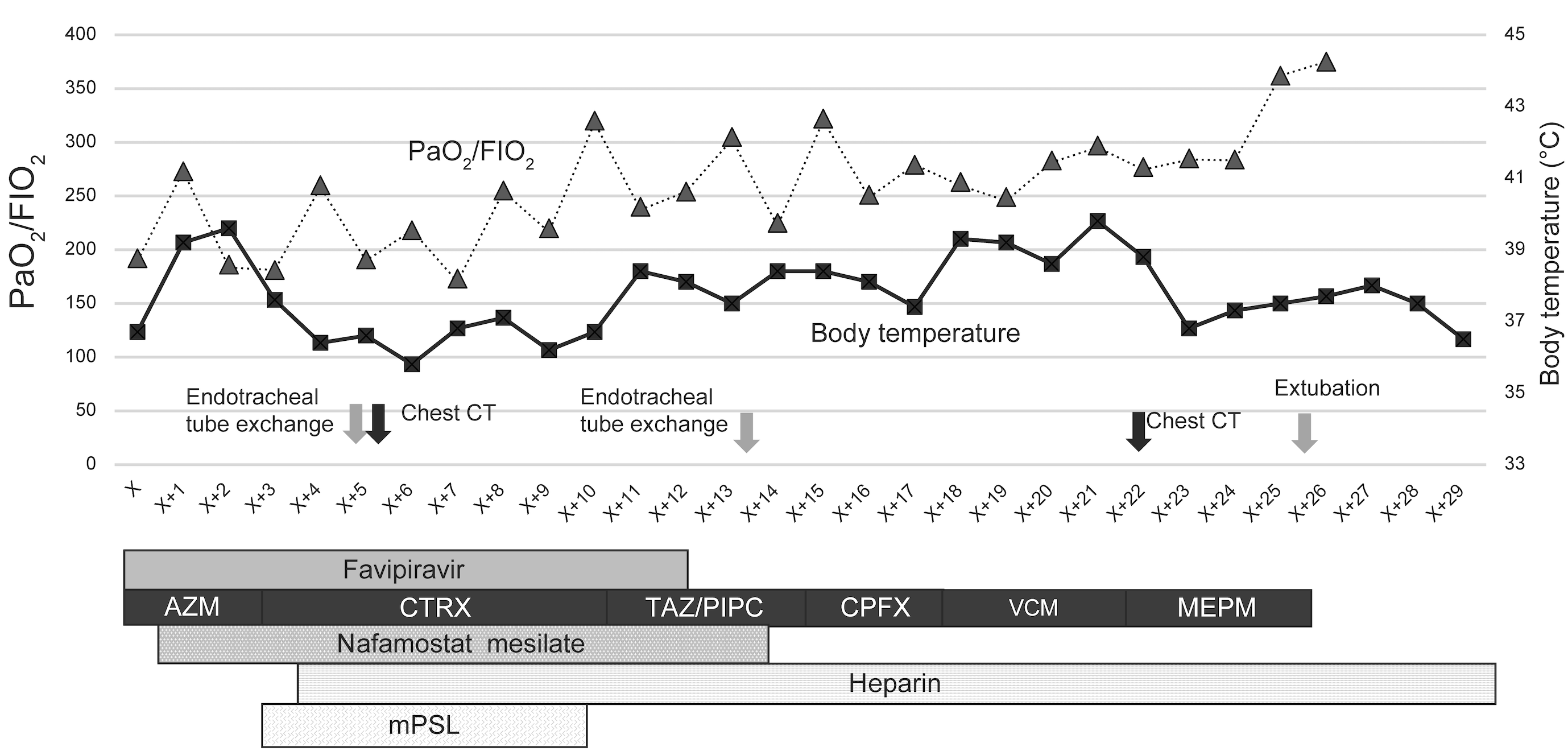
図3 臨床経過:PaO2/FIO2比
緩徐な経過でPaO2/FIO2の改善がみられた。
AZM:azithromycin,CTRX:ceftriaxone,CPFX:cefepime,MEPM:meropenem,mPSL:methylprednisolone,TAZ/PIPC:tazobactam/piperacillin,VCM:vancomycin
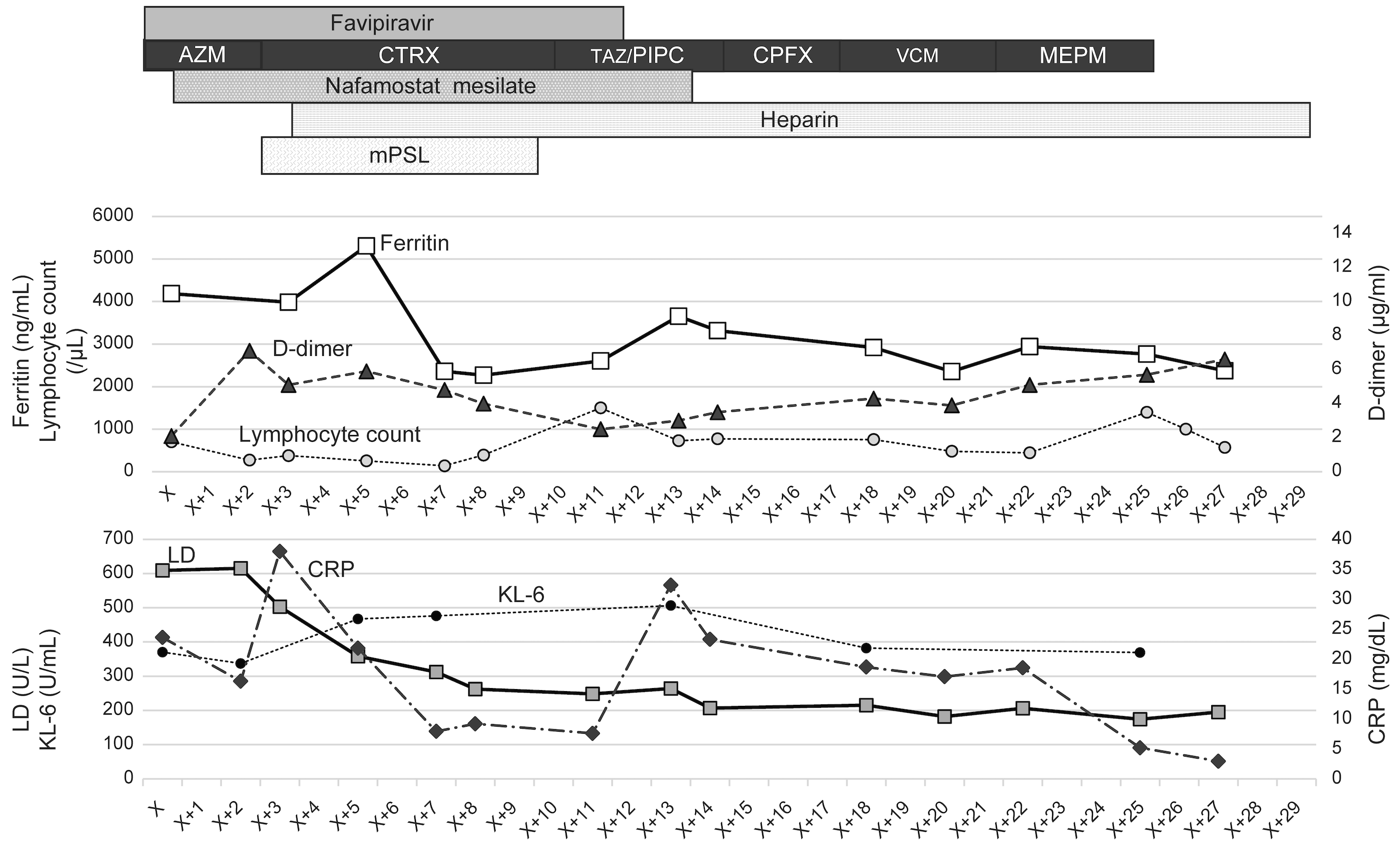
図4 臨床経過:炎症マーカー
CRP・フェリチンは発症初期とX−13日に上昇を認めた。治療経過に伴い上記炎症マーカーのほか,LDやKL-6などのマーカーも低下した.
AZM:azithromycin,CTRX:ceftriaxone,CPFX:cefepime,MEPM:meropenem,mPSL:methylprednisolone,TAZ/PIPC:tazobactam/piperacillin,VCM:vancomycin,CRP:c-reactive protein,LD:lactate dehydrogenase,KL-6:krebs von den lungen-6
本症例はARDSを来した重症COVID-19の1例であったが,適切な呼吸管理・COVID-19に対する治療により呼吸状態の改善が得られた。医療者への二次感染を防ぐ目的で気管切開を避けたが,長期挿管管理にもかかわらず抜管することができた。
重症COVID-19の症例は重篤な転帰をたどることが知られている。中国で行われた72,314例のCOVID-19患者を対象としたケースシリーズでは,5%に重症症例がみられ,その49.0%が死亡したと報告された[2]。本症例もP/F比の低下が著しい重症例で,ARDS中等症の診断となった。
COVID-19によるARDSの概念の1つにL型,H型の分類が報告されている[3]。炎症の進行による肺の血管透過性の亢進・肺水腫のため,L型からH型へ移行し,コンプライアンスの低下を来す。H型へ移行した判定は難しく,本症例でもP/F比の低下や画像所見からは治療抵抗性のH型となった可能性が否定できなかった。
今回抜管できた要因の1つとして,COVID-19に対する呼吸管理が奏効したことが考えられる。H型では換気を増加すると肺への負荷・血流が増加し,時間経過とともにサイトカイン放出や右室過負荷が生じ,全身の臓器機能障害を来し,炎症や浮腫を誘発する。そのためH型では重症ARDSとしての管理を要し,高PEEP・低換気による呼吸補助や腹臥位療法など,従来の肺保護戦略の有効性が示唆されている[4]。今回の治療でも高PEEPによる呼吸補助を行い,X+8日以降はP/F比200以上を維持することができた。本症例では診療当時SARS-CoV-2の感染性が十分に判明しておらず医療者への感染リスクが懸念され,腹臥位など積極的な体位変換ができずチェアポジションまでの介入にとどめた。しかし,一般的なARDSの管理においてチェアポジションであってもP/F比の改善が得られている報告もあり,本症例でも体位変換が無気肺の改善・痰の喀出を促し,酸素化の改善に寄与したものと考えられた[5]。
COVID-19の治療においてファビピラビルやヘパリン,ナファモスタットの観察研究における有効性は報告されており,本症例でも改善に寄与した可能性がある[6][7][8]。本症例の治療当時,ステロイドのエビデンスは報告がなかった。しかし,その後COVID-19患者へデキサメタゾンを投与したことで28日死亡率が低下する報告がなされた[9]。本症例の治療経過でもメチルプレドニゾロン投与後からフェリチンやLDH,P/F比などのマーカーが改善していることから,ステロイドによるCOVID-19への病勢改善効果が得られたものと考えられた。
患者の呼吸状態ならびにCOVID-19・ARDSの病勢は安定したが,呼吸管理の上で気管切開を行うべきか検討が必要であった。一般的に気管切開を行う時期については定まっていない[10]が,喉頭浮腫など上気道合併症や人工呼吸器関連肺炎などのリスクを回避するため,長期挿管管理を要する患者であれば気管切開を考慮する。しかしCOVID-19の場合,侵襲的処置によるエアロゾル発生のため医療従事者が感染するリスクが考えられた。2003年SARS-coronavirus発生時,医療従事者の中でエアロゾル発生処置を行った者と行わなかった者の感染リスクを比較したレビューでは,行った者が気管挿管例で6.6倍,気管切開例で4.2倍高くなることが報告された[11]。SARS-CoV-2の感染性に関するデータは乏しいが,エアロゾル感染に限らずCOVID-19の診療に携わった医療従事者の感染・死亡例は報告されている[12]。診療当時はSARS-CoV-2の感染性が十分にわかっていなかったこともあり,医療従事者への二次感染予防の観点から気管切開ができる状況ではなかった。しかし,COVID-19患者の気管切開について報告がなされ,ウイルス感染後16〜30日程度ではSARS-CoV-2の感染性が低下しており,その時点での気管切開が検討されること,また,喉頭障害や鎮静剤の累積効果,患者とのコミュニケーションなどの点からは早期の気管切開も提案されることが挙げられている[13]。