白石直敬,笠松丈人,前田光一
奈良県総合医療センター感染症内科(〒603-8581 奈良県奈良市七条西町2-897-5)
A case of COVID-19 and Legionella pneumonia co-infection in a young woman
Naoyuki Shiraishi, Takehito Kasamatsu, Koichi Maeda
Infectious Diseases Department, Nara Prefecture General Medical Center, Nara
Keywords:COVID-19,レジオネラ肺炎,共感染,若年女性/COVID-19, Legionella pneumonia, co-infection, young woman
呼吸臨床 2024年8巻7号 論文No. e00194
Jpn Open J Respir Med 2024 Vol. 8 No. 7 Article No.e00194
DOI: 10.24557/kokyurinsho.8.e00194
受付日:2024年4月23日
掲載日:2024年7月25日
©️Naoyuki Shiraishi, et al. 本論文はクリエイティブ・コモンズ・ライセンスに準拠し,CC-BY-SA(原作者のクレジット[氏名,作品タイトルなど]を表示し,改変した場合には元の作品と同じCCライセンス[このライセンス]で公開することを主な条件に,営利目的での二次利用も許可されるCCライセンス)のライセンシングとなります。詳しくはクリエイティブ・コモンズ・ジャパンのサイト(https://creativecommons.jp/)をご覧ください。
主訴:呼吸困難,咳嗽。
既往歴:肺炎(2歳,4歳時)。
内服歴:なし。
職業:大学1年生。
生活歴:友人1人とルームシェア中。
現病歴:X−5日嘔吐後に咽頭違和感を自覚した。X−4日近医を受診し,含嗽薬を処方された。X−3日咳嗽が出現し,呼吸困難を自覚した。その後徐々に呼吸困難が増強したため,X日救急要請し,前医に搬送された。鼻咽頭ぬぐい液によるSARS-CoV-2 PCR陽性が判明し,胸部CT(図1)で両側性の多発肺炎像を指摘された。SpO2 91%(室内気)と低酸素も認められたことから精査加療目的で当院に転送された。1年以上前に2回目COVID-19ワクチン接種を受けた。入浴施設利用歴,旅行歴,農作業従事歴はなく,周囲に冷却塔はない。
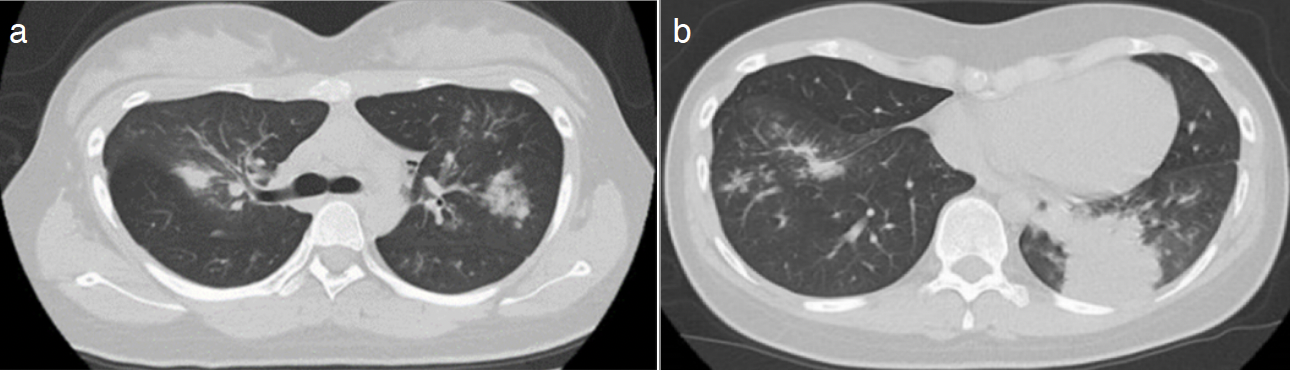
図1 前医の胸部CT像
a. 両側肺野に多発粒状影,多発すりガラス影を認めた。
b. 左下葉背側のすりガラス影の内部に境界明瞭な浸潤影を認めた。
入院時現症:意識レベルE4V5M6,体温37.8℃,血圧93/63mmHg,脈拍120bpm,呼吸回数34回/分,SpO2 94%(O2 4L/分 鼻カヌラ),項部硬直は陰性であった。胸部聴診で心音は整・純,呼吸音は両側で湿性ラ音を聴取した。
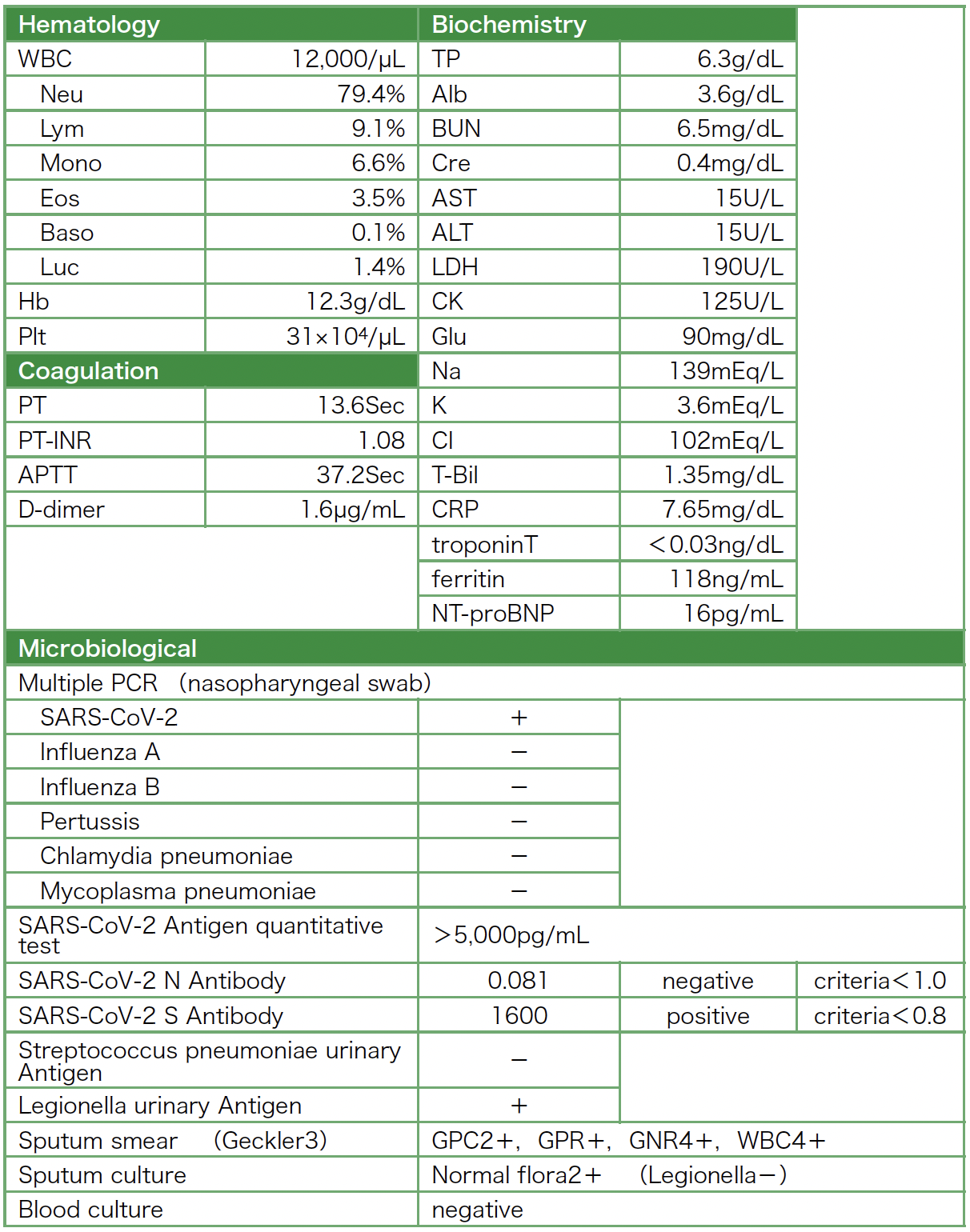
入院時検査所見(表1):白血球数は増加し,CRP高値,D-dimer高値であった。多項目PCRでSARS-CoV-2が陽性であり,SARS-CoV-2抗原定量も強陽性であった。喀痰培養,血液培養では有意所見は認められなかったが,尿中レジオネラ抗原陽性が認められた。
表1 入院時検査所見
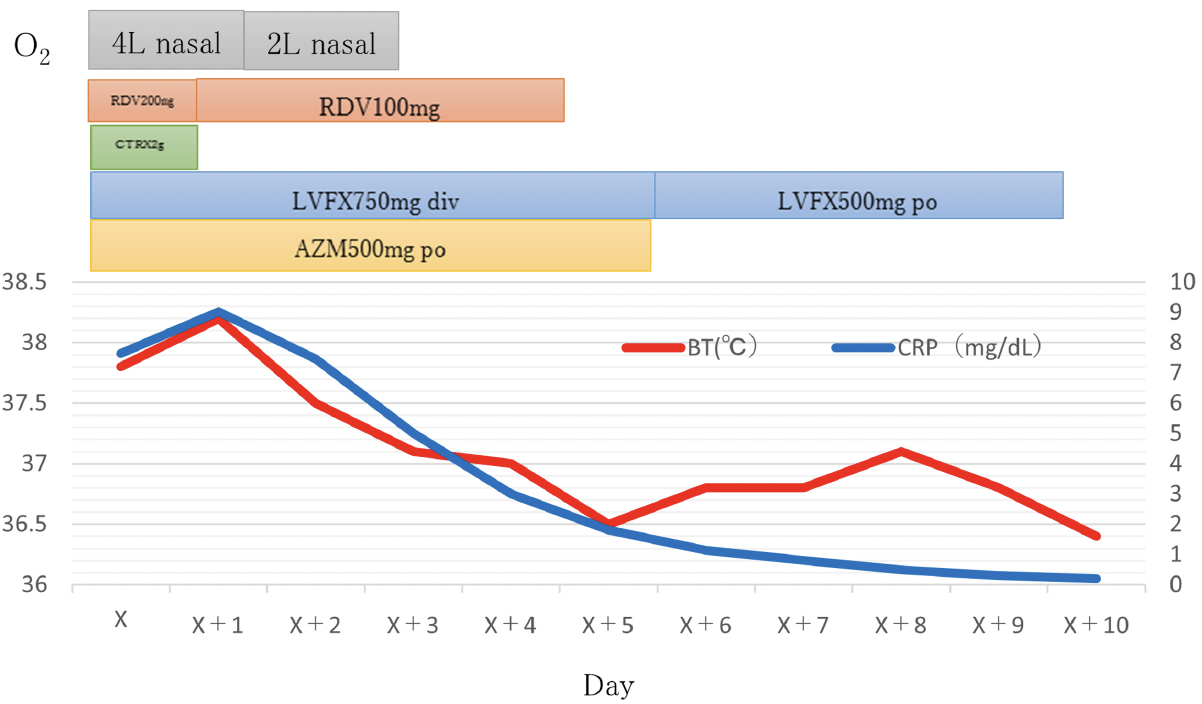
入院後経過(図2):COVID-19に合併したレジオネラ肺炎と診断し,レムデシビル(RDV)を開始し,細菌性肺炎についてはレジオネラ肺炎を中心に考え,レボフロキサシン(LVFX)750mg/日点滴を選択した。シナジー効果が期待される報告があったためアジスロマイシン(AZM)500mg/日内服を併用した[1]。また尿中肺炎球菌抗原は陰性であったが肺炎球菌肺炎合併の可能性を否定できないと考え,キノロン耐性肺炎球菌肺炎をカバーすべくセフトリアキソン(CTRX)2g/日点滴を追加した。喀痰塗抹所見から肺炎球菌肺炎合併の可能性は低いと判断し,X日でCTRXを終了した。経過は良好であり,X+4日酸素吸入を終了,X+5日平熱化し,LVFXを内服に切り替え,AZMを終了した。胸部X線像の経過(図3)でもX+6日に改善が確認された。X+9日CRPが陰転化し,トランスアミナーゼ軽度上昇(AST 32U/L,ALT 32U/L),好酸球上昇傾向(20.5%)のため抗菌薬治療を終了した。X+10日退院となった。
図2 入院後経過
RDV:Remdesivir,LVFX:Levofloxacin,AZM:Azithromycin,CTRX:Ceftriaxone
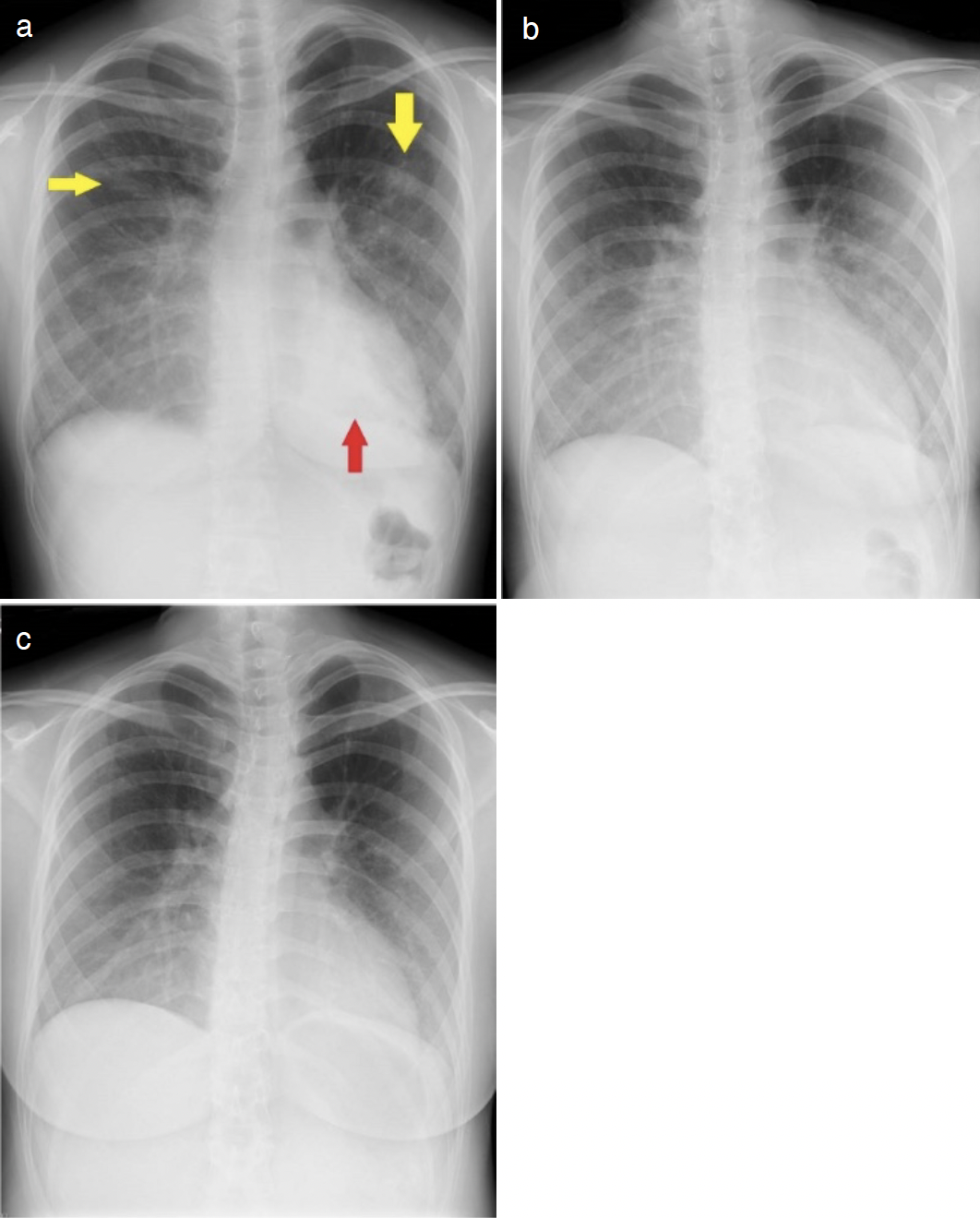
図3 胸部X線像の経過
a. (day X):両側中肺野に索状影(黄矢印),心陰影と重なる浸潤影(赤矢印)を認めた。
b. (day X+2)
c. (day X+6):両側中肺野の索状影,心陰影と重なる浸潤影はほぼ消失している。
COVID-19感染とレジオネラ肺炎の合併の報告は少ない。NakagawaraらはCOVID-19入院患者1,863名のうち140名に呼吸器細菌共感染が認められたと報告しているがLegionella pneumophilaは1件認められたのみだった[2]。Riccoらの報告では10,936名のCOVID-19陽性者のうち,5035名に対し尿中レジオネラ抗原検査,もしくはレジオネラPCR検査が行われたが,陽性者は18名(0.36%)と少なく,うち男性が84.2%,平均年齢61.9歳(35〜83歳,最年少は35歳男性)と若年女性は認められていない[3]。さらにレジオネラ肺炎単独でも,レジオネラ肺炎102例のうち,女性は12例(11.8%),平均年齢67歳(55〜70歳)と若年女性の報告例はなかった[4]。
レジオネラの検査については,2003年より尿中レジオネラ抗原検査が保険適用となり急速に一般化した。従来用いられてきた尿中抗原検査キットは原因菌として最も多いL. pneumophila 血清型1のリポ多糖体に対する抗体を利用していたため,それ以外の血清型によるレジオネラ症の診断が困難であった。2019年血清型1に対する抗体に加え,L. pneumophilaのリボゾーム蛋白L7/L12に対する抗体を利用した尿中抗原検査が開発され,L. pneumophila血清型1〜15のすべてとLegionella dumoffii,Legionella bozemanaeの診断が可能になった。レジオネラ肺炎の原因菌のうちL. pneumophilaは68.0%であり,そのうち血清型1は45.2%を占めるとの報告があるが[5],新しい検査キットにより血清型1以外のレジオネラ肺炎の早期診断が期待されている。
本症例では後者の尿中抗原検査キット(リボテスト®)が陽性であったが,喀痰培養検査は陰性であった。従来の尿中抗原検査キットの特異度は90%台後半と非常に高かったが,リボテスト®の添付文書では既承認品に対し,陽性一致率96.1%,陰性一致率90.0%と記載されており,特異度は90%程度と考えられる。感度が上がった分,特異度はやや低下しており偽陽性の可能性も否定できない。一方で喀痰培養検査についてはレジオネラ肺炎患者のうち50%は痰が出ないと報告されており[6],喀痰培養陽性率も16.7%と低い[7]。本症例でも実際に排痰困難であり,なんとか採取した痰も膿性成分が少なく,検査に適した痰ではなかったためにレジオネラが分離されなかった可能性が高いと考えた。
次にレジオネラ肺炎の画像所見について考察する。本症例では低酸素は来していたものの,前医の胸部CTではCOVID-19肺炎に特徴的な胸膜側優位のすりガラス影は認められず,多発粒状影,斑状影,すりガラス影とともに左下葉背側にすりガラス影の内部に境界明瞭なコンソリデーションが認められた。SakaiらはCTでは非区域性のすりガラス影に混在する,気管支血管束周囲に分布する境界明瞭で直線的なコンソリデーションが特徴的としている[8]。多発斑状影,粒状影は気管支肺炎のパターンであり,典型的なレジオネラ肺炎像ではないが,左下葉背側のすりガラス影の内部の境界明朗なコンソリデーションはレジオネラ肺炎に矛盾しない所見である。発症初期であったことから気管支肺炎パターンと肺胞性肺炎パターンが混在していた可能性を考えた。
レジオネラ症の宿主の危険因子として,男性,喫煙者,慢性心疾患,慢性肺疾患,糖尿病,慢性腎不全患者,移植患者,免疫抑制状態にある患者,担癌患者,50歳以上などが挙がるが[9],COVID-19重症化リスク因子と合致する点が多く,COVID-19感染者の中からレジオネラ肺炎合併例を見落とさないように留意すべきである。さらにCOVID-19肺炎ではステロイド,バリシチニブ,トシリズマブなどの免疫抑制薬が投与されることがあるが,レジオネラ肺炎合併が見逃されカバーされていなければ重症化する可能性があり特に注意が必要である。
主な感染経路としては,レジオネラ属菌を含んだエアロゾル(感染性エアロゾル)や,土壌の粉塵の吸入とされており,冷却塔,入浴施設,建設現場等で使用される機械,配管システム,医療機関における人工呼吸器の使用,園芸・農業,津波災害等に関連した症例や集団発生の報告がある[10]。国立感染症研究所の2011年第1週~2021年第35週のレジオネラ症の届出状況によると,感染原因・感染経路(確定・推定)は16,841例中水系感染が5,465例(全報告に占める割合:32.5%),塵埃感染が953例(5.7%)(重複例もあり)とされているが,不明例も多い。本症例も感染経路は不明であり,ルームメイトもCOVID-19感染は認められたが,レジオネラ感染は認められていない。
Miyashitaらはレジオネラ肺炎予測スコアとして男性,咳嗽なし,呼吸困難あり,CRP≧18mg/dL,Na<134mmol/L,LDH≧260U/Lをそれぞれ1点とし,カットオフ値を3点以上とした場合,感度93%,特異度75%と報告しており,さらに109人の市中レジオネラ肺炎患者は全て2点以上であったとも報告している[11]。本症例は呼吸困難のみの1点であり,非典型例であったと言える。レジオネラ肺炎の好発年齢でなく,感染を疑うエピソードがない場合であっても,臨床経過,検査データ,画像所見などからレジオネラ共感染の可能性が否定できない場合は積極的に検査を行うべきである。本症例では画像上肺抱性肺炎を呈していたことから肺炎球菌肺炎と共にレジオネラ肺炎を鑑別疾患として挙げた。
レジオネラ肺炎の治療については,βラクタム系抗菌薬が無効であり,また急速に重症化する可能性があることから,早期診断,早期治療介入が肝要である。致死率は初診から診断までの期間が1日の場合1.0%,5〜7日で3.5%,8日以上で4.6%と報告されている[12]。本症例では入院時低酸素のため4Lの酸素需要があったものの,早期診断,早期治療介入により経過は良好であった。
利益相反なし。
The case was a 19-year-old female who had been healthy all her life. She was brought to the previous hospital due to breathing difficulties, and was found to be SARS-CoV-2 PCR positive, with multiple pneumonia images shown in Chest CT, and suffering from hypoxia, so she was transferred to our hospital for further investigation and treatment. We suspected that she had not only COVID-19 infection but also bacterial pneumonia based on CT findings, and after various tests were performed, her urine was positive for Legionella antigen. An early diagnosis of co-infection with COVID-19 and Legionella pneumonia was made, and she improved with appropriate treatment in a short time.