瀧 玲子*1,鴨志田達彦*2,佐藤希美*1,八巻春那*1,小澤達志*1,東 盛志*1,髙山幸二*1,花田仁子*1,小島勝雄*3,市村浩一*4
*1武蔵野赤十字病院呼吸器科(〒180-8610 東京都武蔵野市境南町1-26-1)
*2横須賀共済病院呼吸器内科
*3唐津赤十字病院呼吸器外科
*4いちむら内科クリニック
A case of congenital pulmonary airway malformation discovered in adulthood
Reiko Taki*1, Tatsuhiko Kamoshida*2, Nozomi Sato*1, Haruna Yamaki*1, Tatsushi Kozawa*1, Seishi Higashi*1, Koji Takayama*1, Satoko Hanada*1, Katsuo Kojima*3, Koichi Ichimura*4
*1Department of Respiratory Medicine, Japanese Red Cross Musashino Hospital
*2Department of Respiratory Medicine, Yokosuka Kyosai Hospital
*3Department of Thoracic Surgery, Japanese Red Cross Karatsu Hospital
*4Ichimura Clinic
Keywords:先天性肺気道奇形,成人,感染性肺囊胞,部分切除/congenital pulmonary airway malformation (CPAM), adult, infectious lung cyst, wedge resection
呼吸臨床 2023年7巻5号 論文No.e00172
Jpn Open J Respir Med 2023 Vol. 7 No. 5 Article No.e00172
DOI: 10.24557/kokyurinsho.7.e00172
受付日:2023年3月12日
掲載日:2023年5月22日
©️Reiko Taki, et al. 本論文はクリエイティブ・コモンズ・ライセンスに準拠し,CC-BY-SA(原作者のクレジット[氏名,作品タイトルなど]を表示し,改変した場合には元の作品と同じCCライセンス[このライセンス]で公開することを主な条件に,営利目的での二次利用も許可されるCCライセンス)のライセンシングとなります。詳しくはクリエイティブ・コモンズ・ジャパンのサイト(https://creativecommons.jp/)をご覧ください。
患者:54歳,女性。
主訴:発熱。
既往歴:48歳時に子宮筋腫子宮全摘,50歳頃から気管支喘息。
生活歴:喫煙歴5本/日(20歳〜24歳),飲酒歴なし。
家族歴:特記事項なし。
現病歴:X-3年健診胸部X線写真では異常を指摘されなかった。X-2年健診胸部X線写真で異常陰影指摘され当科紹介受診,胸部CTで右下葉S6に多房性囊胞性病変を認めたが無症状でありいったん経過観察となった。また気管支喘息については,吸入ステロイド+長時間作用型β2刺激薬を中心とした標準治療をしていたが,しばしば増悪を繰り返していた。X-1年秋,発熱,膿性痰が出現し,囊胞内感染と診断され抗菌薬内服でいったん軽快したが,以後も感染を繰り返すため感染性囊胞として手術の方針となり,X年6月入院となった。
身体所見:身長159cm,体重52.9kg,体温36.2℃,血圧128/78mmHg,脈拍68回/分・整,呼吸数14回/分,SpO2 97%(室内気),呼吸音清でラ音聴取せず。
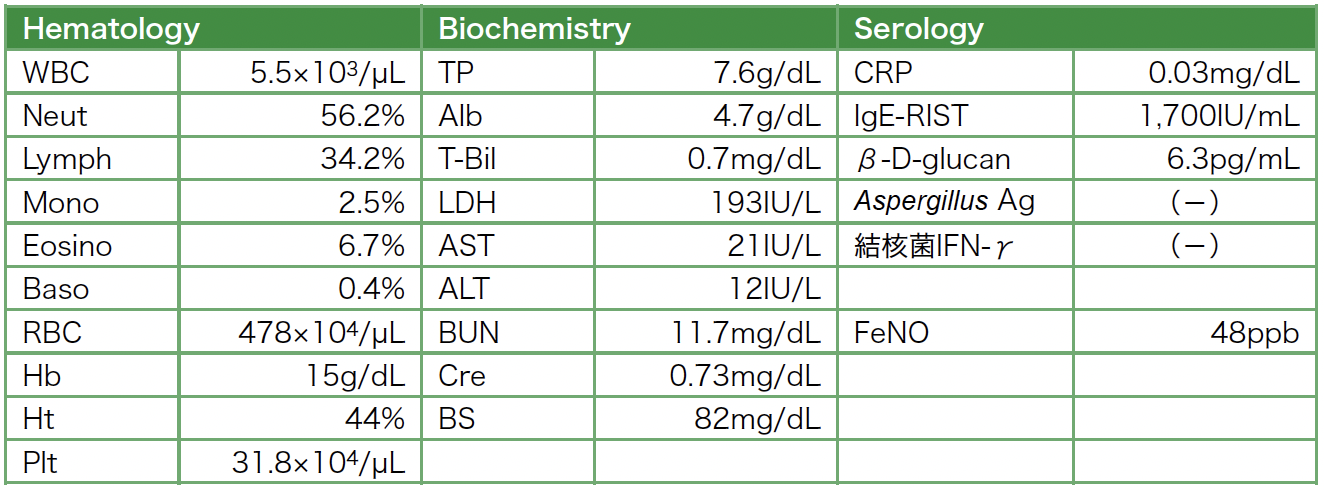
入院時検査所見(表1):血液検査ではWBC 5,500/μL,CRP 0.03mg/dLと炎症反応は陰性であり,IgE-RIST 1,700 IU/mLと高値を認めた。
画像所見:X-2年当科初診時の胸部X線写真(図1a)では,右下肺野縦隔側に鏡面像を伴う囊胞性病変を認めていたが,X年術前X線写真(図1b)では,鏡面像は消失していた。また,X-1.5年胸部造影CT(図2a,b)では右肺下葉縦隔側に径50mmの多房性囊胞性病変を認め,液体貯留はほとんど認めなかった。中枢側気管支の閉塞所見なく,また大動脈からの異常血管を認めず,気管支閉鎖症や肺分画症は否定的であった。X年術前CT(図2c)では囊胞の拡大と囊胞周囲にすりガラス陰影の出現を認めた。
表1 入院時検査所見
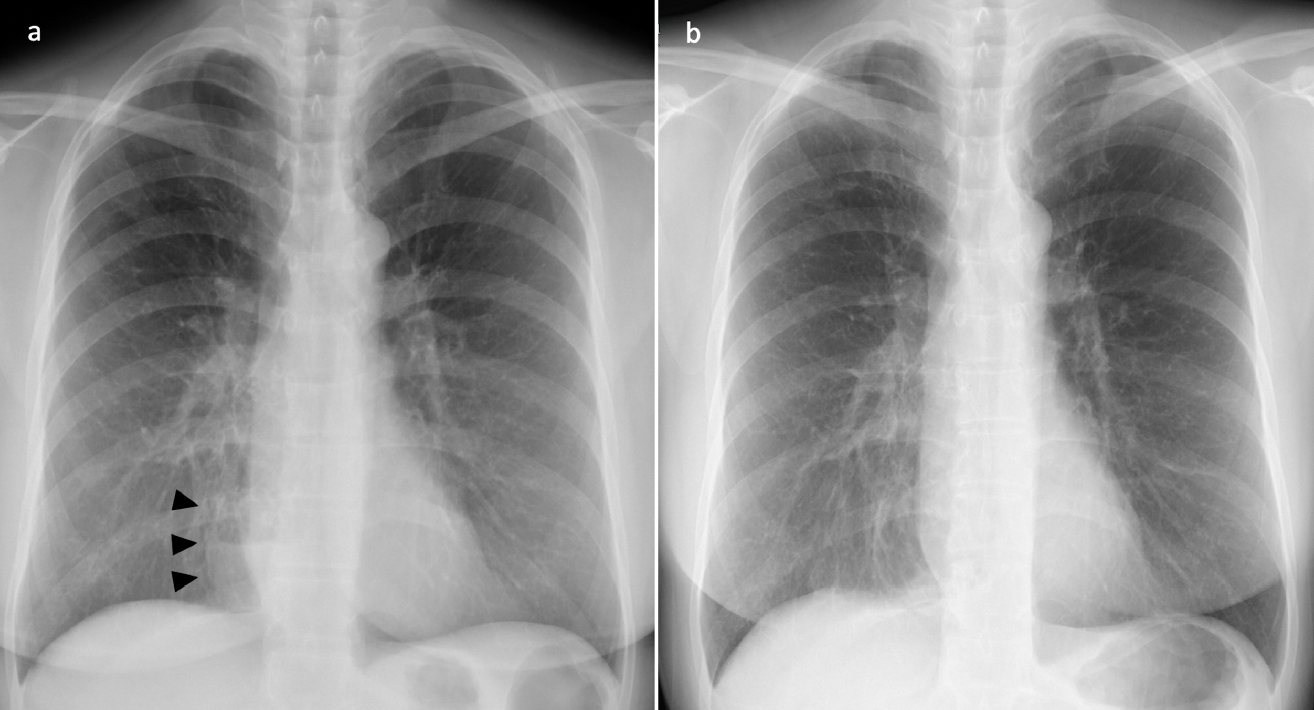
図1 胸部X線写真
X-2年(a)では,右下肺野縦隔側に鏡面像を伴う囊胞性病変を認めるが(矢頭),X年術前(b)には,鏡面像は消退していた。
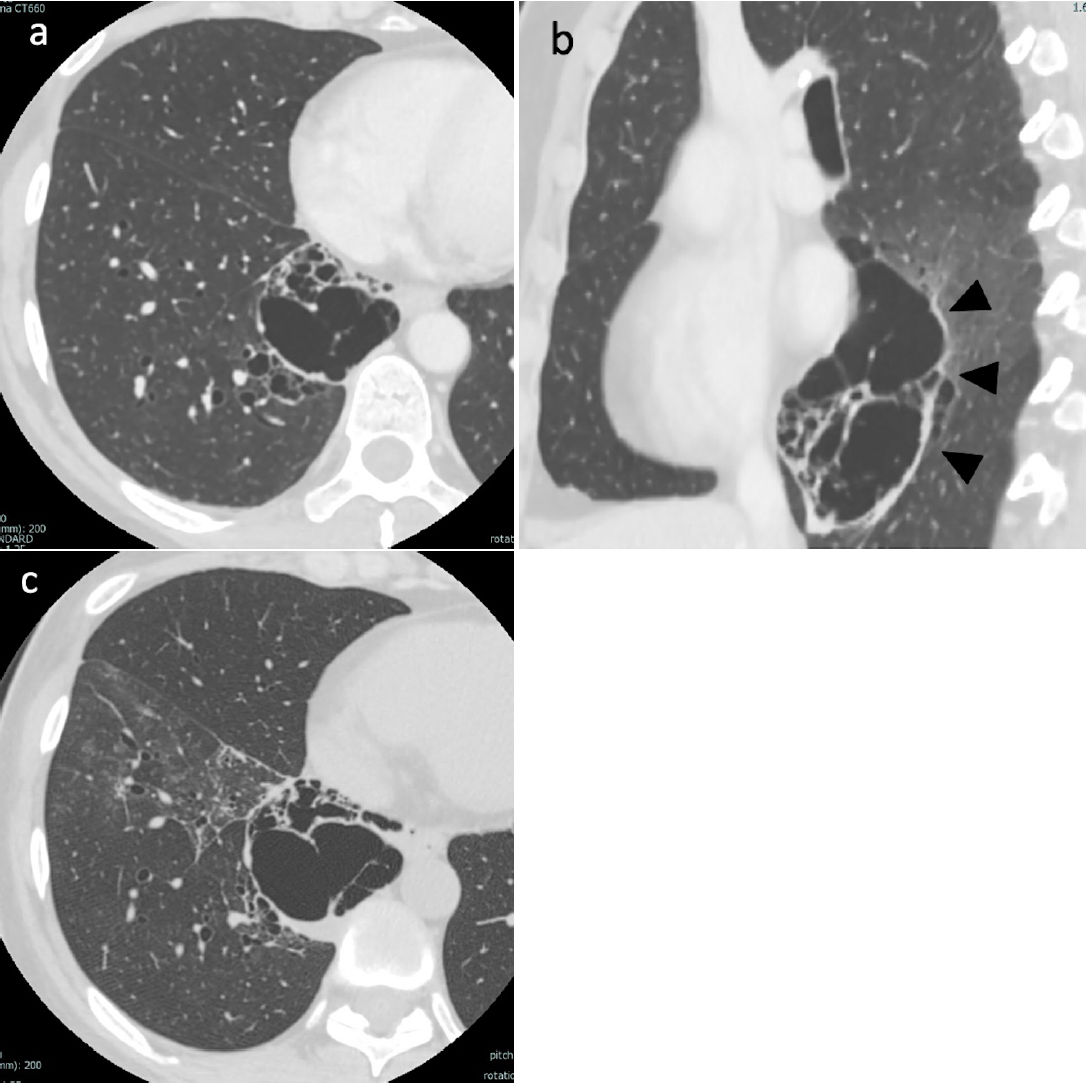
図2 CT写真
X-1.5年胸部造影CT(a,b)では右肺下葉縦隔側に径50mmの多房性囊胞性病変を認め(矢頭),X年術前CT(c)では囊胞の拡大と囊胞周囲にすりガラス陰影の出現を認めた。
手術所見:小開創および2-port胸腔鏡で実施,胸腔内は下葉―胸壁間,肺尖―胸壁間で癒着が目立ち,S6c〜S10の広範囲な領域で径60mmの囊胞を認めた。囊胞内部には白色粘稠な内容物を,また上下葉間の胸膜および囊胞壁表面の一部に毛細血管の増生を認め,炎症の既往が示唆された。癒着および下肺静脈周囲を剝離し囊胞を含む肺部分切除を施行した。
病理組織所見:肉眼的には肺実質内に多房性囊胞性病変を認めた(図3a)。顕微鏡的には病変は弱拡大において30mm大までの大小多数の拡張囊胞と線維性間質からなり,囊胞内に粘液産生を認めた。強拡大では囊胞内腔の大部分は多列線毛円柱上皮で被覆され,間質に著明なリンパ球・形質細胞浸潤を認めたが,細菌・真菌感染を示唆する所見は認めなかった(図3b,c)。また別の部位では,PAS-Alcian blue染色陽性の粘液産生細胞を認めた(図3d,e)。
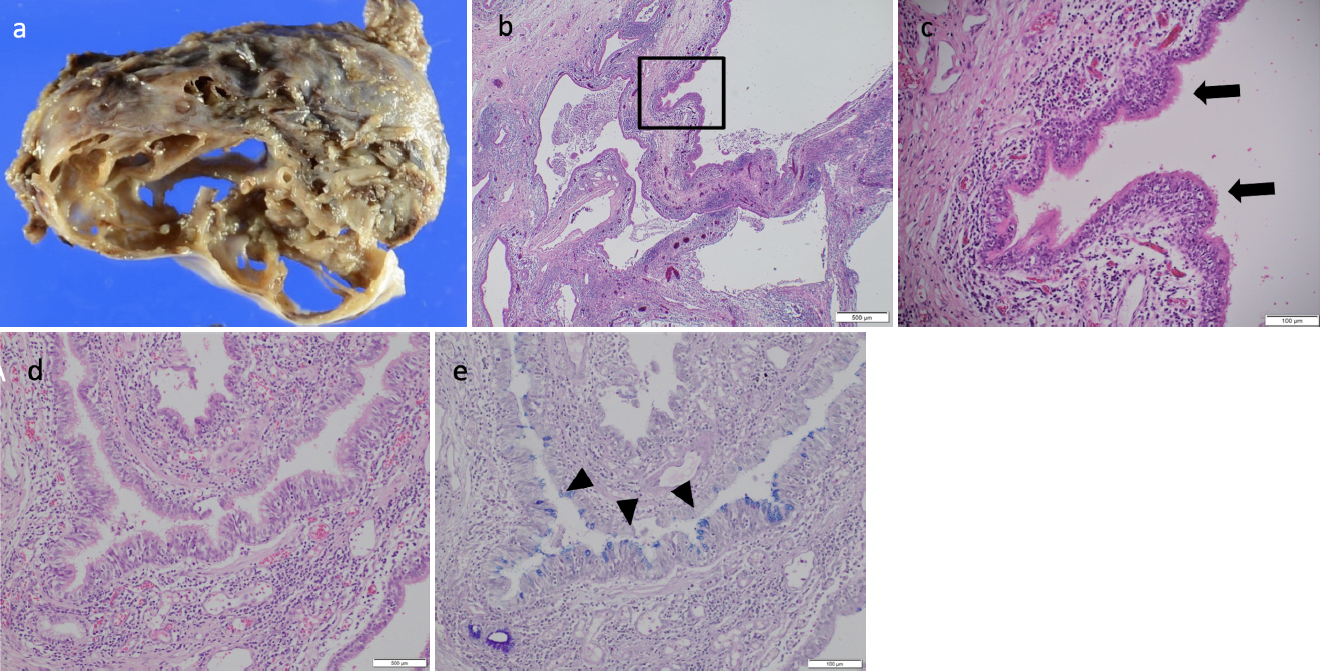
図3 病理所見
a. 肉眼的病理所見:肺実質内に多房性囊胞病変を認める。
b. 顕微鏡所見(弱拡大):粘液産生を伴う大小多数の囊胞を認める。
c. 顕微鏡所見(強拡大):囊胞壁の大部分は多列線毛円柱上皮で被覆されていた(矢印)。
d,e. 別の部位では,PAS-Alcian blue染色陽性の粘液産生細胞を認めた(矢頭)。
以上の病理所見と画像所見より,CPAMの60〜70%を占め最も一般的な形態であるCPAM Type Iと診断した。経過良好で術後約7年の現在まで気道感染の合併は認めていない。また気管支喘息についても,2型炎症は存在しているが,IgE-RIST(術前1,700 IU/mL→術後7年1,100 IU/mL),末梢血好酸球数(369/μL→148/μL),FeNO(48ppb→38ppb)と,いずれもやや低下し,生活環境には変化がないがまったく増悪がなくなった。治療はstep downし,ほぼ無治療で経過観察している。
CPAMは以前先天性囊胞性腺腫様奇形(congenital cystic adenomatoid malformation:CCAM)として知られていたまれな先天性囊胞性疾患の1つである。1977年Stockerらは,囊胞壁の上皮が増殖して腺腫様所見を呈する38例を分析し,CCAMは発生過程における過誤腫的病変であり,囊胞の大きさなどに基づきType I〜Ⅲに分類されると報告した[1]。その後,当初の過誤腫様の気道上皮増殖に病因を求めたCCAMの概念を捨て,発生過程で気道のいずれかのレベルで発生が停止もしくは遅延した場合囊胞が形成されるとする新たな病因論と概念を提唱し,0型,Ⅳ型を加え,5型からなるCPAMという新たな呼称を与えた[2]。
CPAMは,現在約80%の症例が胎児期の超音波検査や,新生児期の呼吸不全で発見,診断されている[3]。このため,本症例のような54歳という成人期での診断例はまれとされているが,Hamanakaらは61例の成人例のレビューを報告しており[3],近年症例は集積されてきている。その中でも我々の症例より高年齢の症例は9例と少なく,無症状であったのは胸部CT異常陰影にて発見され手術で診断された肺癌合併の80歳1例のみで[4],他は呼吸器症状を契機に発見されている。本症例ではX-3年の健診時まで異常を指摘されず,54歳で初めて発見され診断に至った。その原因として,第一に右下葉縦隔側の薄壁囊胞であり,X線写真では縦隔に重なってわかりにくい位置であったこと,第二に手術までの2年間に囊胞が増大傾向にあることから以前はより小さく判別が難しかったと推測されること,などが考えられる。さらに,手術所見では胸壁との癒着や囊胞壁表面の毛細血管増生,病理組織所見では間質の炎症細胞浸潤など,過去の炎症や慢性炎症を示唆する所見を認めたものの,健診で異常を指摘されるまでは明らかな感染症の既往がなく,CTでの精査の機会がなかったことも発見を遅らせた一因になったと考えた。
囊胞性肺疾患には,肺の形成過程で異常が発生して起こるCPAM等の気管支性肺囊胞,炎症や瘢痕などにより胸膜の近くに発生する気腫性肺囊胞,さらにリンパ脈管筋腫症,ランゲルハンス細胞組織球症など肺の内部に多発囊胞を認める疾患などがあり鑑別が必要である[5]。本症例は胸部X線写真では鏡面像を伴う薄壁囊胞であり,感染性肺囊胞(気腫性肺囊胞)と術前診断し,肺部分切除術を施行し術後CPAMの診断に至った。囊胞性肺疾患については,CTで肺の一葉に多房性囊胞があり血管走行が正常な時にはまれな疾患ではあるがCPAMを考慮すべき[6],とされており,本症例はCTでは単発性の多房性囊胞を呈しており,気管支性肺囊胞の鑑別が必要であった。
成人期のCPAMの治療については,先天性囊胞性肺疾患診療ガイドライン[7]では定められていないが,有症状の患者には一般的に外科的切除が推奨されている。一方無症状の患者の治療についても,残存病変による感染の再燃のリスクやまれではあるが悪性腫瘍の発生のリスクがあるため,多くの場合病変の切除が推奨されている[8]。術式については,多くの報告例[3][9]で肺葉切除が行われている一方で,CTで囊胞が限局して,壁肥厚や結節など悪性を疑う所見を伴わずに完全切除可能と判断されたときには,初回は部分切除や区域切除で十分であるとの意見もある[3]。本症例では,術前には感染性肺囊胞の診断であったが感染がコントロールできていたこと,囊胞が右下葉胸膜直下に位置する限局性病変であり,近傍の下肺静脈との間が剝離できれば完全切除可能と判断したこと,腫瘍を疑う結節所見を伴わなかったこと,また気管支喘息の合併があり肺機能の温存を重視したこと等から肺部分切除を選択した。術後CPAMとの病理診断後,54歳という年齢も考慮して追加切除せずに慎重に経過観察の方針としたが,術後約7年経過している現在,残存肺を含めて気道感染などの合併を認めていない。
さらに,本症例では術後,気管支喘息症状が著明に改善した。血清IgE-RIST高値,呼気NO高値,聴診上狭窄音を聴取し気道可逆性を認め,成人発症の気管支喘息と確定診断しておりCPAMとは独立した併存疾患であるが,以前からの喘息の繰り返す増悪は,CPAMによる気道感染症状が顕在化する以前から囊胞内に生じた感染が繰り返し気管支を刺激していたことが一因であったと考えた。CPAMでは囊胞が気管支を通じて外界と交通しているため,交通を持たない気管支閉鎖症や肺分画症に比べて感染するリスクは高いと考えられている[10]。経過中に胸部X線写真で囊胞内の鏡面形成が自然減少したこともあり,鏡面像は潜在的な感染を反映していると考えられた。
また,成人期CPAMと肺癌の合併について,Lantuejoulら[11]はCPAMを画像診断後,3年,10年の無治療経過観察で肺内転移を来して肺腺癌合併と診断された2例を,またChangらは[12]部分切除後7年後に再発した浸潤性粘液性腺癌合併例を報告している。画像診断では癌の合併の判別が困難なことも多く,CPAMでの粘液細胞は以前の組織分類での粘液性細気管支肺胞上皮癌の前駆病変と見なされるべきである[13]という意見もある。CPAMは肉眼的に囊胞と正常肺組織との境界は判別困難であり,主病巣の囊胞と離れた一見正常肺と見られる組織内に小囊胞がみられたという症例の報告[9]もある。本症例では,CPAM病変に肺癌の合併は認めず,画像上残存病変も認めていないが,部分切除であり今後も慎重に経過観察する予定である。
The patient is a 54-year-old woman with bronchial asthma. She was diagnosed with a cystic lung lesion through a computed tomography scan and followed up as asymptomatic. Subsequently, she underwent lung wedge resection for infectious lung cysts due to repeated respiratory infections and was diagnosed with congenital pulmonary airway malformation (CPAM). Seven years post-surgery, no recurrence of airway infection or bronchial asthma attacks have occurred, and the patient is doing well.
It has been reported that CPAM is rarely detected at a relatively old age. Since there have been reports of complications such as infection and malignancy, it is advisable to consider this disease when cystic lung lesions occur and to select treatment methods based on age and complications.