須賀 淳*1,中村雄介*1,古屋秀和*2,中川知己*1,山口雅臣*2,山田俊介*1,岩﨑正之*3
*1東海大学医学部付属八王子病院呼吸器外科(〒192-0032 東京都八王子市石川町1838),*2同心臓血管外科
*3東海大学医学部外科学系呼吸器外科学
A case of thymic carcinoma complicated by aortic stenosis for which surgery was performed simultaneously
Atsushi Suga*1, Yusuke Nakamura*1, Hidekazu Furuya*2, Tomoki Nakagawa*1, Masaomi Yamaguchi*2, Shunsuke Yamada*1, Masayuki Iwazaki*3
*1 General Thoracic Surgery, *2 Cardiovascular Surgery, Tokai University Hachioji, Hospital, Tokyo
*3 Division of General Thoracic Surgery, Department of Surgery, Tokai University School of Medicine, Kanagawa
Keywords:前縦隔腫瘍,胸腺癌,大動脈弁狭窄症/anterior mediastinal tumor, thymic carcinoma, aortic stenosis
呼吸臨床 2021年5巻4号 論文No.e00122
Jpn Open J Respir Med 2021 Vol. 5 No. 4 Article No.e00122
DOI: 10.24557/kokyurinsho.5.e00122
受付日:2021年2月21日
掲載日:2021年4月23日
©️Atsushi Suga, et al. 本論文はクリエイティブ・コモンズ・ライセンスに準拠し,CC-BY-SA(原作者のクレジット[氏名,作品タイトルなど]を表示し,改変した場合には元の作品と同じCCライセンス[このライセンス]で公開することを主な条件に,営利目的での二次利用も許可されるCCライセンス)のライセンシングとなります。詳しくはクリエイティブ・コモンズ・ジャパンのサイト(https://creativecommons.jp/)をご覧ください。
症例:70歳,女性。
主訴:胸部異常陰影。
現病歴:健診で心雑音を指摘され大動脈弁狭窄症(aortic stenosis:AS)を疑い精査中,前縦隔腫瘍を指摘され当院に紹介となった。自覚症状は認めていない。
既往歴:特記事項なし。
喫煙歴:なし。
身体所見:身長151cm,体重46kg,体温36.0℃,血圧120/70mmHg,脈拍93回/分・整。胸部聴診で第2肋間胸骨右縁にLevine III/VI度の収縮期雑音を聴取。
胸部単純X線写真:正面像で病変指摘困難,側面像で前縦隔領域に透過性低下を認めた。
胸部CT:上行大動脈前面に5.1cmの造影効果を伴う境界明瞭な腫瘤を認めた(図1)。
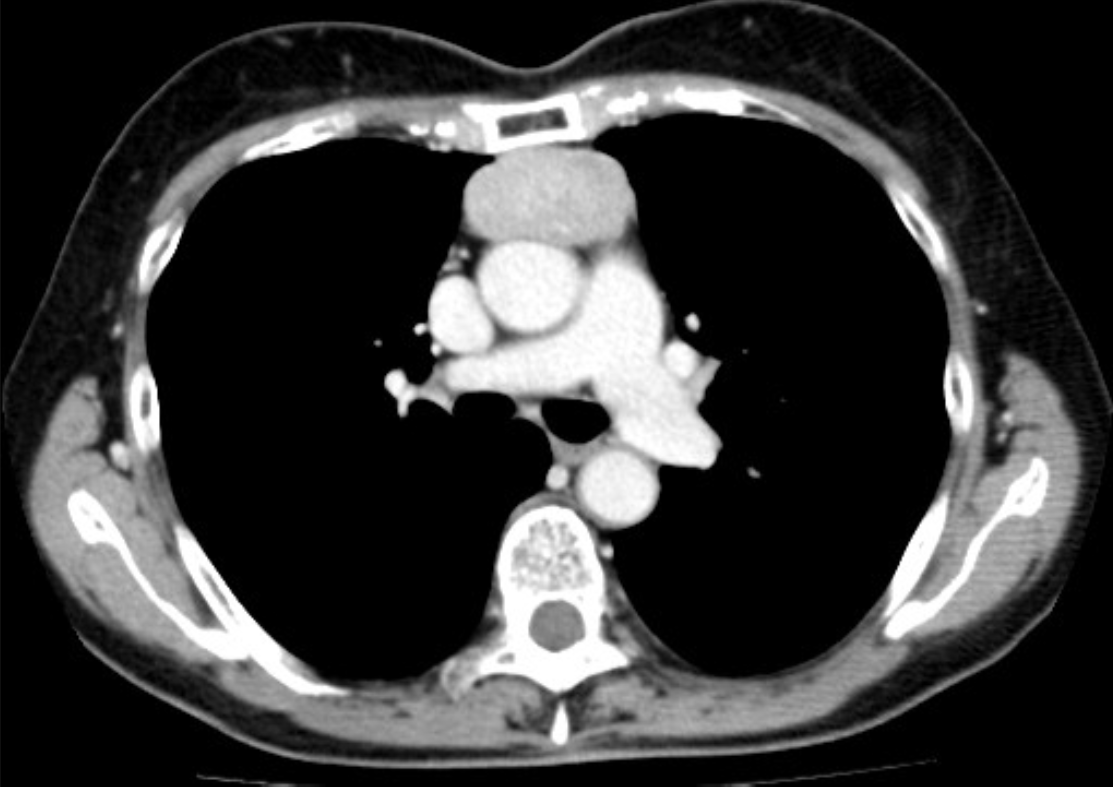
図1 胸部CT
上行大動脈前面に5.1cmの造影効果を伴う腫瘤を認めた。
胸部MRI:腫瘤はT1強調画像で低信号,T2強調画像で筋肉より高信号を呈した。
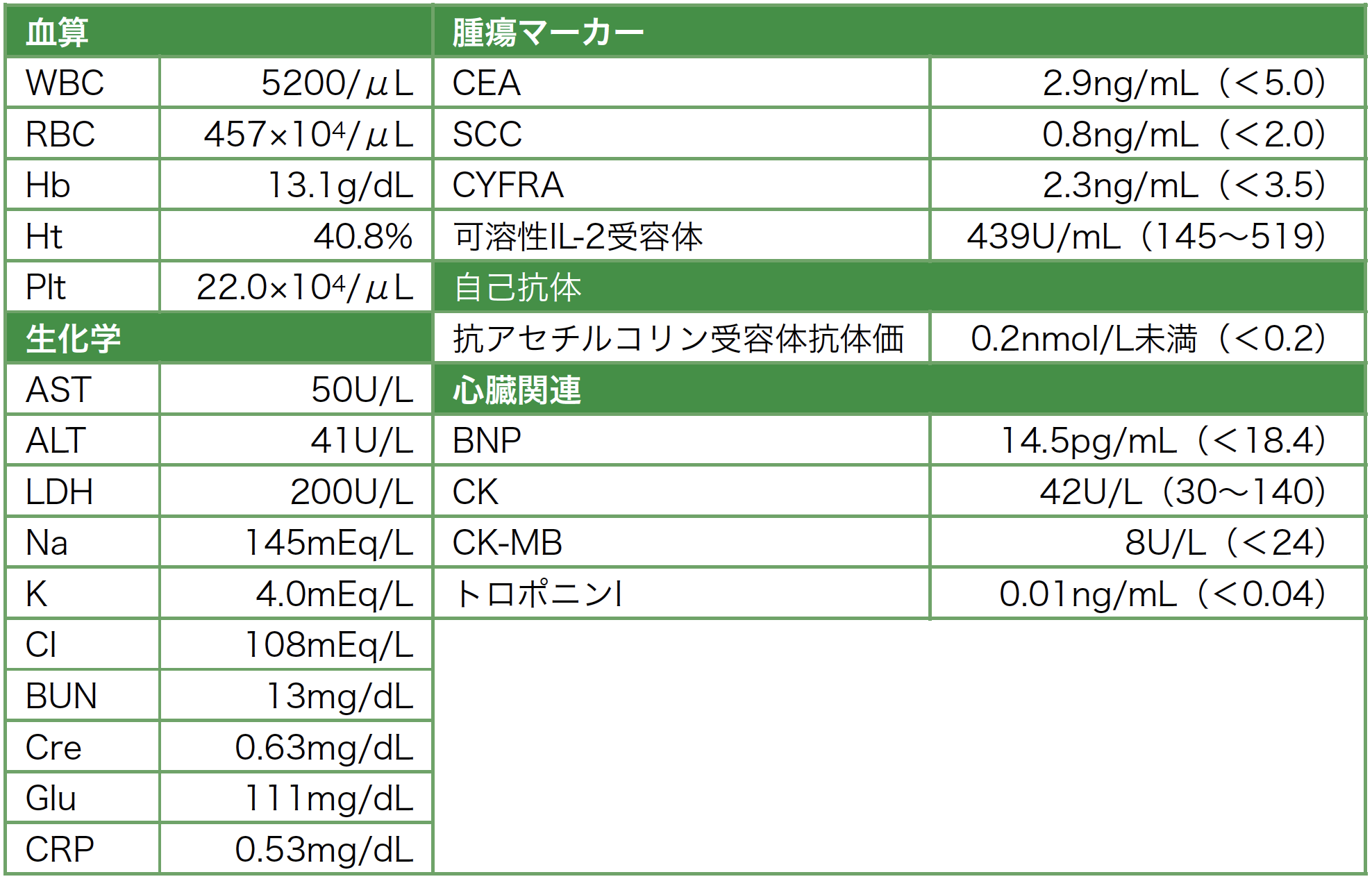
血液・生化学所見:肝酵素の軽度上昇を認めたが腫瘍マーカーの上昇は認めなかった(表1)。
表1 血液生化学,腫瘍マーカー
心電図:安静時心電図は異常所見なく,トレッドミル運動負荷心電図では4METsでST低下を認めた。
心臓超音波検査所見:大動脈弁弁口面積(トレース法)0.76cm2,弁口面積係数0.42cm2/m2,左室-大動脈間平均圧較差33mmHg,大動脈弁通過最高流速4.0m/秒で高度ASの所見を示していたが,左室駆出率61%で壁運動と僧帽弁は正常であった。
冠動脈CT:有意狭窄なし。
以上より高度ASを伴う切除可能な胸腺腫を疑い胸骨正中切開による一期的手術を選択した。
手術所見:胸腺を含めて胸腺脂肪織を剝離すると腫瘍は心膜に癒着しており,癒着部は腫瘍と共に合併切除した。黄色透明の心囊液を細胞診に提出。次いで体外循環下で生体弁を用い大動脈弁置換術を施行し,心膜切除部位はePTFEシートで補填した。
病理診断:肉眼的には腫瘍の境界は明瞭であったが,組織学的には辺縁部に被膜形成がなく,硝子化線維性間質で囲まれた腫瘍胞巣は周囲に浸潤性に増殖し,心膜への浸潤を認めた(図2)。低分化型の扁平上皮癌と診断。心囊液細胞診はclass Vで,病期は正岡分類[1]でIVa期,UICC TNM分類でT2N0M1a stage IVAであった。術後補助化学療法としてカルボプラチンとパクリタキセルを6コース投与。術後2年現在無再発経過観察中である。
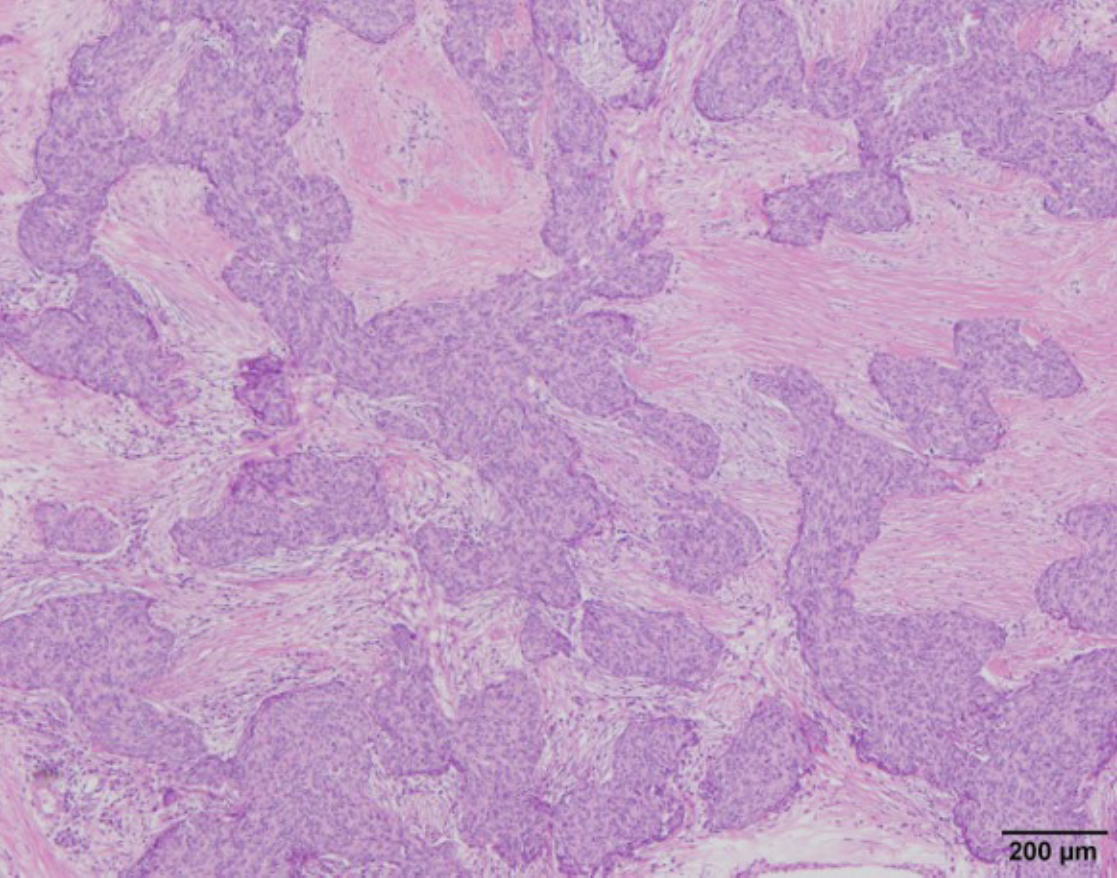
図2 病理組織所見
硝子化した線維性間質で囲まれた腫瘍胞巣が浸潤性に増殖していた。リンパ球は少数で形質細胞の浸潤を認めた。免疫組織化学ではCD5陽性,CD117陽性,MUC-1陽性で周囲のリンパ球にTdT陽性細胞は見られなかった。以上より胸腺癌で扁平上皮癌と診断した。
ASの原因として先天性二尖大動脈弁,リウマチ,炎症等があり,約80%が加齢による退行性変化による。その病態は大動脈弁の狭窄により左室の流出路が狭小化し圧負荷が加わり左室と大動脈間に圧較差が生じ,左室は求心性肥大を来す。その結果左室のコンプライアンスが低下し拡張不全となり拡張期圧が上昇し左室への血液の流入が障害され,心拍出量の維持ができず心不全を呈する。心臓の拡張障害は同時に冠血流が減少しさらに心筋肥大が加わり相対的心筋虚血となり狭心症,不整脈や血圧低下による失神を来しうる。上記の経過は緩徐に進行するため本症例のように機能的に重症(大動脈弁通過最高流速≧4.0m/秒もしくは平均圧較差≧40mmHg,大動脈弁口面積(AVA)≦1.0cm2:弁膜症治療のガイドラインJCS2020による)であっても無症状で経過するが,ASに伴う自覚症状出現後は数年以内に突然死に至る[2]。そのため患者に併存疾患による非心臓手術を行う際には,病巣切除による身体への負担やリスク,治療予後に加えて患者の心疾患の病態を理解することが重要となる。
本症例は心臓超音波検査で高度AS所見を呈するが,自覚症状がなく,まだ左室駆出率は正常で左室のコンプライアンスは保てた状態であった。冠動脈に問題なく,既往に腎機能障害,脳血管疾患,糖尿病等の危険因子がないことを考慮すれば,AAH・AHAガイドラインによると縦隔腫瘍手術は中程度リスクの手術にあたり中止基準とならない[3][4]。縦隔病巣は画像上切除可能な胸腺腫を疑い,胸腔鏡下で胸腺摘出術の単独手術も考えた。トレッドミル運動負荷心電図では4METsでST低下を認め,階段を昇る程度の運動負荷により心筋虚血の所見を呈したことより,周術期に心筋虚血となるリスクがある点と,画像所見で腫瘍径が5.1cmと大きく浸潤性胸腺腫の可能性があり,胸骨正中切開であれば腫瘍切除術から大動脈弁置換術への一連の手術操作が可能である。また大動脈弁置換術手術の自体の周術期死亡率は2.4%である[2]。胸腺腫単独手術した場合の予後が見込めること[5]を考えれば,将来ASに対する手術が必要になることがあるかもしれない。一方,腫瘍の不完全切除時や再発時,ASを伴う心疾患に対して化学療法や放射線療法を施行する際の有害事象,同様の報告例を考慮して腫瘍切除と弁置換術の一期的な手術が適切と判断した[6][7]。
胸腺癌は胸腺上皮腫瘍の14%と頻度が少なく[5],胸腺腫と比較して隣接臓器への浸潤が強い傾向にあり予後不良である。自験例は,術前CTで境界が明瞭な縦隔に限局した病巣であり,胸腺癌により多く認める壊死像,出血等の所見に乏しく広範に広がる浸潤所見を認めていない[8]。手術所見を含めて術直後は心膜浸潤を伴う胸腺腫(正岡分類III期)で根治的手術症例(R0)と考えていたが術後の病理所見の結果で心膜浸潤を伴う胸腺癌(低分化の扁平上皮癌)で心囊液細胞診class Vの非切除症例(正岡分類:IVa期,TNM分類:T2N0M1a stage IVA)であることが判明した。胸腺癌の化学療法に関して議論はあるが,比較的良好と報告されているカルボプラチンとパクリタキセルを6コース施行[9]。術後2年,無再発経過観察中である。今回われわれは高度ASに伴う前縦隔腫瘍を経験した。結果的にはR1(顕微鏡的腫瘍残存)で完全切除不能例の胸腺癌であったが,高齢化社会で今後増加が予想されるASに対し,合併した前縦隔腫瘍への適切な外科的治療での対処法は,呼吸器外科領域の診療において重要と考え報告した。
本論文の要旨は第179回日本胸部外科学会関東甲信越地方会(2019年3月,東京)で発表した。
利益相反の有無:開示すべき利益相反はない。
A 70-year-old woman was found to have a heart murmur during her annual medical examination, and she was diagnosed with aortic stenosis. A 51-mm-diameter anterior mediastinal tumor suspected to be a thymoma was detected at that time. Computed tomography showed that the tumor was located in front of the ascending aorta. Because she had no apparent symptoms of aortic stenosis, we assessed the aortic stenosis as a relative indication for the operation. Preoperatively, we considered that the tumor might be easily resected because it was located within the same field as that for open heart surgery. Therefore, we performed simultaneous thymectomy and aortic valve replacement. Because the tumor was adhered to the pericardium, we partially resected the pericardium. The patient’s postoperative course was uneventful, and no complications occurred. The final pathological diagnosis was thymic squamous cell carcinoma. Because the cytologic examination of the pericardial effusion indicated class V, she subsequently received chemotherapy for the thymic carcinoma. She had not developed recurrence by 2 years postoperatively.